题目内容
在一定温度下的恒容密闭容器中发生的可逆反应2NO2(g)?N2O4(g),下列说法不正确的是( )
| A、容器内压强不再变化,可说明达到化学平衡 |
| B、混合气体的颜色不再变化,可说明达到化学平衡 |
| C、达到平衡时,正逆反应仍然在进行 |
| D、若有2mol NO2放入密闭容器中,必生成1mol N2O4 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:反应到达平衡状态时,正逆反应速率相等,平衡时各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,平衡为动态平衡,由此进行判断.
解答:
解:A.反应前后气体分子数不等,故反应过程中压强变化,若压强不变,反应达到平衡状态,故A正确;
B.二氧化氮红棕色,四氧化二氮为无色,反应过程中颜色在变化,当颜色不变,则达到平衡状态,故N正确;
C.化学平衡为动态平衡,正逆反应速率相等但不为0,故C正确;
D.可逆反应不能进行到底,故2mol NO2放入密闭容器中,生成的N2O4小于1mol,故D错误,
故选D.
B.二氧化氮红棕色,四氧化二氮为无色,反应过程中颜色在变化,当颜色不变,则达到平衡状态,故N正确;
C.化学平衡为动态平衡,正逆反应速率相等但不为0,故C正确;
D.可逆反应不能进行到底,故2mol NO2放入密闭容器中,生成的N2O4小于1mol,故D错误,
故选D.
点评:本题考查了化学平衡状态的判断.分析反应过程的变化量,该变的量若保持不变,则反应达到平衡状态,依次可快速判断平衡状态.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
NO和CO都是汽车尾气里的有害物质,它们能缓慢反应,生成氮气和二氧化碳,对此反应,下列叙述正确的是( )
| A、使用催化剂不改变反应速率 |
| B、改变温度对反应速率无影响 |
| C、升高温度能加快反应速率 |
| D、使用催化剂能加快反应速率 |
在反应:H2+CuO
H2O+Cu中,H2作( )
| ||
| A、还原剂 | B、氧化剂 |
| C、还原产物 | D、氧化产物 |
下列物质是电解质的是( )
| A、Fe |
| B、SO3 |
| C、K2SO4 |
| D、C12H22O11(蔗糖) |
下列有关实验操作正确的是( )
A、 称量氢氧化钠固体 |
B、 检验铁粉与水蒸气反应产生的氢气 |
C、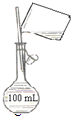 配制150mL 0.10 mol?L-1盐酸 |
D、 分离两种沸点相差较大的液体互溶混合物 |