题目内容
4.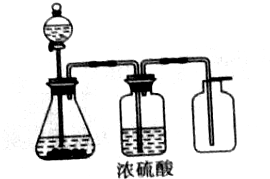 实验室制取、收集干燥的以下6种气体:
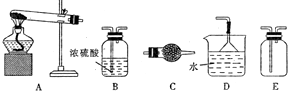
实验室制取、收集干燥的以下6种气体:①CO2②H2S ③NO2④O2⑤Cl2 ⑥NH3
如图装置可适用的气体是①②③④⑥;制取装置不适用的是⑤;干燥装置不适用的是②⑥;收集装置不适用的是⑥.
分析 由图可知,反应由固体和液体在常温下反应生成气体,生成的气体可用于浓硫酸干燥,且用向上排空法收集,说明气体的密度比空气大,以此解答该题.
解答 解:反应由固体和液体在常温下反应生成气体,可用于制备①CO2(可用碳酸钙和盐酸)②H2S (FeS和稀硫酸)③NO2(浓硝酸和铜)④O2(二氧化锰和双氧水)⑥NH3(浓氨水和碱石灰),不适用于⑤Cl2(二氧化锰和浓盐酸)的制备,应在加热条件下进行,由于浓硫酸具有酸性和强氧化性,不适于干燥②H2S、⑥NH3,用向上排空法收集,说明气体的密度比空气大,则不适用于⑥NH3,
故答案为:①②③④⑥;⑤;②⑥;⑥.
点评 本题综合考查常见气体的制备、干燥和收集,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及实验的方法、原理、注意事项,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.有如下四种物质:①CH2═CH2、②CH≡CH、③ 、④HCHO.下列说法正确的是( )
、④HCHO.下列说法正确的是( )
 、④HCHO.下列说法正确的是( )
、④HCHO.下列说法正确的是( )| A. | 四种物质分子中,碳原子都是采取sp2杂化 | |
| B. | HCHO分子的空间构型为平面三角型,且分子中含有4个σ键 | |
| C. | 四种物质中所有原子都在同一平面内 | |
| D. | ①②两种有机物与H2发生加成反应时分子中的所有化学键发生断裂 |
15.在一定温度下,溶剂不变的密闭容器中发生反应A(g)+B(s)?C(g)+D(g),下列不能说明该可逆反应已经达到平衡状态的是( )
| A. | 混合气体压强不再发生变化 | |
| B. | 混合气体质量不再发生变化 | |
| C. | A的物质的量浓度不变 | |
| D. | 单位时间里生成C(g)和D(g)的物质的量相等 |
12.有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D导线C;③A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应.据此,判断四种金属的活动性顺序是( )
| A. | A>B>C>D | B. | A>C>D>B | C. | C>A>D>B | D. | C>B>D>A |
9.下列反应中会有沉淀产生的是( )
| A. | 将二氧化硫气体通入酸性KMnO4溶液中 | |
| B. | 将二氧化硫气体通入碘水中 | |
| C. | 将二氧化硫气体通入BaCl2溶液中 | |
| D. | 将少量二氧化硫气体通入Ba(OH)2溶液中 |
2.下表给出了X、Y、Z、W四种短周期元素的部分信息,请根据这些信息判断下列说法中正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径/nm | 0.102 | 0.16 | 0.074 | 0.071 |
| 最高正价或最低负价 | +6 | +2 | -2 | -1 |
| A. | 原子序数X>Y>Z>W | B. | 纯净的X与纯净的Z反应生成XZ3 | ||
| C. | Z的最高正价为+6 | D. | HW是热稳定性最强的氢化物 |
19.乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,存在与自然界的植物中,其晶体(H2C2O4•2H2O)无色,101℃开始熔化,易溶于水,受热脱水、升华,170℃时开始分解,其钠盐和钾盐易溶于水.而其钙盐难溶于水.
(1)依据表中给出的数据判断下列化学方程式可能正确的是BD(填序号)
两种多元酸是电离常数(25℃)
A.H2C2O4+CO32-═HCO3-+HC2O4-
B.HC2O4-+CO32-═HCO3-+C2O4-
C.2C2O4-+CO2+H2O═2HC2O4-+CO32-
D.H2C2O4+CO32-═C2O42-+H2O+CO2↑
(2)某化学兴趣小组的同学选用如图所示的部分装置(可以重复选用)进行商业,验证草酸的分解产物(已知:H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O↑)

如果气体流向为从左到右,装置依次连接的合理顺序为ACBDFDGHDI.
(3)草酸溶液能使酸性高锰酸钾溶液褪色,其反应历程为:

①称取3.2g草酸晶体,配制250mL0.10mol/LH2C2O4溶液
②在上述过程中必须用到的2种定量仪器是托盘天平和250mL容量瓶.
③下列操作会使所配溶液浓度偏高的是B(填序号)
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘
B.定容时俯视刻度线
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
④写出草酸溶液与酸性KMnO4溶液反应的离子方程式:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
⑤由于KMnO4能氧化水中的有机物等因素,为了配制稳定的KMnO4溶液,其浓度需标定,取10.00mL0.10mol/LH2C2O4溶液于锥形瓶中,加入10mL0.50mol/LH2SO4溶液、用KMnO4溶液滴定至锥形瓶中溶液颜色恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00mL,则上述实验中KMnO4溶液的物质的量浓度为0.01mol/L.
(1)依据表中给出的数据判断下列化学方程式可能正确的是BD(填序号)
两种多元酸是电离常数(25℃)
| 弱酸 | H2C2O4 | H2CO3 |
| 电离常数 | K1=5.4×10-2 K2=5.4×10-5 | K1=4.5×10-7 K2=4.7×10-11 |
B.HC2O4-+CO32-═HCO3-+C2O4-
C.2C2O4-+CO2+H2O═2HC2O4-+CO32-
D.H2C2O4+CO32-═C2O42-+H2O+CO2↑
(2)某化学兴趣小组的同学选用如图所示的部分装置(可以重复选用)进行商业,验证草酸的分解产物(已知:H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O↑)

如果气体流向为从左到右,装置依次连接的合理顺序为ACBDFDGHDI.
(3)草酸溶液能使酸性高锰酸钾溶液褪色,其反应历程为:

①称取3.2g草酸晶体,配制250mL0.10mol/LH2C2O4溶液
②在上述过程中必须用到的2种定量仪器是托盘天平和250mL容量瓶.
③下列操作会使所配溶液浓度偏高的是B(填序号)
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘
B.定容时俯视刻度线
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
④写出草酸溶液与酸性KMnO4溶液反应的离子方程式:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
⑤由于KMnO4能氧化水中的有机物等因素,为了配制稳定的KMnO4溶液,其浓度需标定,取10.00mL0.10mol/LH2C2O4溶液于锥形瓶中,加入10mL0.50mol/LH2SO4溶液、用KMnO4溶液滴定至锥形瓶中溶液颜色恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00mL,则上述实验中KMnO4溶液的物质的量浓度为0.01mol/L.
20.下列用连线方法对部分化学知识进行归纳的内容中,有错误的组是( )
| A. | 保护环境:控制“白色污染”--减少和控制使用所有塑料制品防止水的污染--提倡使用无磷洗衣粉 | |
| B. | 基本安全常识:饮用假酒中毒--由甲醇引起食用假盐中毒--由亚硝酸钠引起 | |
| C. | 物质的性质与用途:磺胺类药物能抑制细菌合成核酸--治疗肺炎、脑膜炎、呼吸道感染酸能与碱中和-----胃酸过多的病人服用含氢氧化钠的药物 | |
| D. | 生活中的一些做法:除去衣服上的油污--可用汽油洗涤使煤燃烧更旺--可增大煤与空气接触面积 |