题目内容
12.有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D导线C;③A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应.据此,判断四种金属的活动性顺序是( )| A. | A>B>C>D | B. | A>C>D>B | C. | C>A>D>B | D. | C>B>D>A |
分析 一般来说,原电池中,较活泼的金属作负极、较不活泼的金属作正极,放电时电流从正极流向负极,负极上失电子发生氧化反应、正极上得电子发生还原反应,据此判断金属活动性顺序.
解答 解:①A、B用导线相连后,同时浸入稀硫酸溶液中,A极为负极,所以活泼性:A>B;
②原电池中,电子从负极流经外电路流向正极,C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D,则活泼性:C>D;
③A、C相连后,同时浸入稀硫酸溶液中,C极产生大量气泡,说明C极是正极,所以金属活泼性:A>C;
④B、D相连后,同时浸入稀硫酸溶液中,D极发生氧化反应,说明D极是负极,所以金属活泼性:D>B;
综上可知金属活泼性顺序是:A>C>D>B,B项正确;
故选B.
点评 本题以原电池原理考查金属活动性顺序,侧重考查学生分析判断能力,明确正负极的判断、正负极发生的反应类型、电子或电流流向即可解答,题目难度不大.

练习册系列答案
相关题目
2.下列说法正确的是( )
| A. | 氨基酸、蛋白质、油脂都含有C、H、O、N四种元素 | |
| B. | 乙烯、聚乙烯、甲苯均能使酸性高锰酸钾溶液褪色 | |
| C. | 糖类、油脂和蛋白质均属于高分子化合物 | |
| D. | 在加热、甲醛、饱和CuSO4溶液、X射线作用下,蛋白质都会发生变性 |
3.有关下列物质分子结构特征描述正确的是( )
| A. | 1mol CH3CH2OH与Na完全反应只生成0.5 mol H2,不能说明乙醇分子中有一个氢原子与其它氢原子不同 | |
| B. | 苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构 | |
| C. | 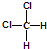 和 和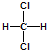 属于同一种物质,不能用来解释甲烷是一种正四面体结构 属于同一种物质,不能用来解释甲烷是一种正四面体结构 | |
| D. | 乙烯容易与溴的四氯化碳溶液发生反应,且1mol乙烯完全加成消耗1mol溴单质,证明乙烯分子里含有一个碳碳双键 |
20.下列物质属于纯净物的是( )
| A. | 乙烷 | B. | 汽油 | C. | 柴油 | D. | 天然气 |
7.下列说法正确的是( )
①NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
②含有共价键的晶体一定具有高的熔、沸点及硬度
③s-s σ键与s-p σ键的电子云形状相同
④含有π键的化合物与只含σ键的化合物的化学性质不同
⑤中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
⑥配位键在形成时,是由成键双方各提供一个电子形成共用电子对.
①NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
②含有共价键的晶体一定具有高的熔、沸点及硬度
③s-s σ键与s-p σ键的电子云形状相同
④含有π键的化合物与只含σ键的化合物的化学性质不同
⑤中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
⑥配位键在形成时,是由成键双方各提供一个电子形成共用电子对.
| A. | ①②⑤ | B. | ①④⑤ | C. | ②③⑤ | D. | ②③⑥ |
17.现有含W g碳酸钙和a g二氧化硅的混合物,在高温下反应最终可生成标准状况下的气体体积为( )
| A. | $\frac{a}{60}×22.4$L | B. | $\frac{W}{100}×22.4$L | C. | $\frac{W-a}{40}×22.4$L | D. | 无法计算 |
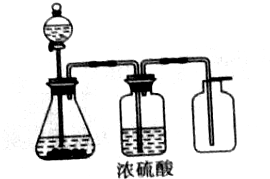 实验室制取、收集干燥的以下6种气体:
实验室制取、收集干燥的以下6种气体: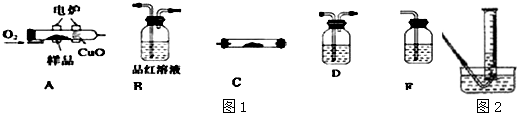
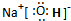 ,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”).