题目内容
16.标准状况下,与22.4ml氧气分子数目相等的氢气的质量为多少?分析 根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$计算,结合分子组成分析.
解答 解:标准状况下,22.4ml氧气的物质的量为$\frac{0.0224L}{22.4L/mol}$=0.001mol,氢气的分子数与氧气相同,则物质的量也相同,所以氢气的物质的量为0.001mol,所以氢气的质量为0.001mol×2g/mol=0.002g;
答:氢气的质量为0.002g.
点评 本题考查了有关物质的量的计算,题目难度不大,注意把握物质的量的有关公式,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.已知强酸与强碱在稀溶液里发生中和反应生成1mol H2O 时放出57.3kJ热量,用500mL 0.6mol•L-1的稀硫酸跟含1mol NaOH的溶液反应,放出的热量是( )
| A. | 68.76 kJ | B. | 57.3 kJ | C. | 34.38 kJ | D. | 17.19 kJ |
4.下列除杂试剂选择正确的是( )
| 物质(杂质) | 除杂试剂 | |
| A | NaHCO3(Na2CO3) | 稀盐酸 |
| B | CO2(HCl) | 饱和碳酸钠溶液 |
| C | NH3(H2O) | 浓硫酸 |
| D | Fe3+(Fe2+) | 过氧化氢溶液 |
| A. | A | B. | B | C. | C | D. | D |
11.广州亚运会期间,广州气象部门的科技人员为了保证亚运会开幕式的正常进行,一直做好“驱雨”准备.所谓“驱雨”就是在“雨云”到达广州之前向其发射装有有关化学物质的“炮弹”,提前将“雨云”转化成雨降下,从而保证广州无雨.催雨剂的主要成分是干冰、液氮、碘化银(AgI)等,下列物质与上述三种物质类别完全不同的是( )
| A. | I2 | B. | K2SO4 | C. | P2O5 | D. | HNO3 |
8.只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是( )
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 甲 | 物质微粒数 | 标准状况下气体摩尔体积 | 固体体积 | 溶液的质量分数 | 非标准状况下物质的质量 |
| 乙 | 阿伏加德罗常数 | 标准状况下气体体积 | 固体密度 | 溶液的体积 | 物质的摩尔质量 |
| A. | ②④ | B. | ④⑤ | C. | ③④ | D. | ③ |
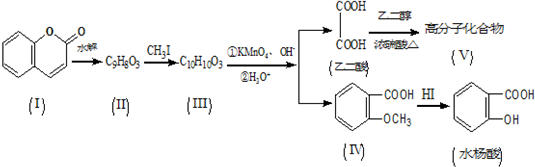
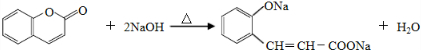 .
.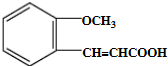 .
. .
.