题目内容
Ⅰ.将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,各物质浓度随时间变化的关系如图1所示.
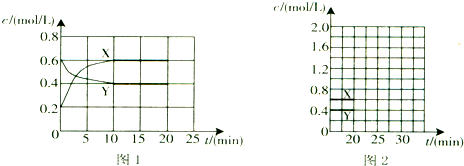
请回答:
(1)下列选项中不能说明该反应已达到平衡状态的是 (填选项字母).
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)反应进行到10min时,共吸收热量11.38kJ,则该反应的热化学方程式为 ;
(3)计算该反应的平衡常数K= .
(4)反应进行到20min时,再向容器内充入一定量NO2,10min后达到新的平衡,此时测得c(NO2)=0.9mol/L.
①第一次平衡时混合气体中NO2的体积分数为w1,达到新平衡后混合气体中NO2的体积分数为w2,则w1 w2(填“>”、“=”或“<”);
②请在图2中画出20min后各物质的浓度随时间变化的曲线(曲线上必须标出“X”和“Y”).
Ⅱ.(1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料.如LiFePO4电池中某电极的工作原理如图所示:
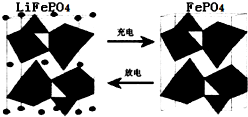
该电池的电解质为能传导Li+的固体材料.放电时该电极是电池的 极(填“正”或“负”),该电极反应式为 .
(2)用此电池电解含有0.1mol/L CuSO4和0.1mol/L NaCl的混合溶液100mL,假如电路中转移了0.02mol e-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是 L.

请回答:
(1)下列选项中不能说明该反应已达到平衡状态的是
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)反应进行到10min时,共吸收热量11.38kJ,则该反应的热化学方程式为
(3)计算该反应的平衡常数K=
(4)反应进行到20min时,再向容器内充入一定量NO2,10min后达到新的平衡,此时测得c(NO2)=0.9mol/L.
①第一次平衡时混合气体中NO2的体积分数为w1,达到新平衡后混合气体中NO2的体积分数为w2,则w1
②请在图2中画出20min后各物质的浓度随时间变化的曲线(曲线上必须标出“X”和“Y”).
Ⅱ.(1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料.如LiFePO4电池中某电极的工作原理如图所示:

该电池的电解质为能传导Li+的固体材料.放电时该电极是电池的
(2)用此电池电解含有0.1mol/L CuSO4和0.1mol/L NaCl的混合溶液100mL,假如电路中转移了0.02mol e-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是
考点:物质的量或浓度随时间的变化曲线,原电池和电解池的工作原理,化学平衡常数的含义,化学平衡状态的判断
专题:化学平衡专题,电化学专题
分析:Ⅰ、(1)化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论;
(2)根据图象进行判断并计算,可得热化学方程式;
(3)根据化学方程式及平衡常数的定义书写;
(4)①增大压强,平衡向着气体体积减小的方向移动;
②根据平衡时浓度作图;
Ⅱ、(1)在原电池放电时,负极上失电子发生氧化反应,正极上得电子发生还原反应,根据得失电子确定正负极,根据反应物、生成物书写电极反应式;
(2)由离子放电顺序可知,电解含有0.01molCuSO4和0.01molNaCl的混合溶液100ml,阳极上氯离子和氢氧根离子放电生成氯气和氧气,2Cl--2e-=Cl2↑,阴极上铜离子得电子,以此计算.
(2)根据图象进行判断并计算,可得热化学方程式;
(3)根据化学方程式及平衡常数的定义书写;
(4)①增大压强,平衡向着气体体积减小的方向移动;
②根据平衡时浓度作图;
Ⅱ、(1)在原电池放电时,负极上失电子发生氧化反应,正极上得电子发生还原反应,根据得失电子确定正负极,根据反应物、生成物书写电极反应式;
(2)由离子放电顺序可知,电解含有0.01molCuSO4和0.01molNaCl的混合溶液100ml,阳极上氯离子和氢氧根离子放电生成氯气和氧气,2Cl--2e-=Cl2↑,阴极上铜离子得电子,以此计算.
解答:
解:(1)A.反应前后气体的化学计量数之和不等,故容器总压强不随时间改变可作为判断是否达到化学平衡状态的依据,故A正确;
B.密度=
,总质量不变,体积也不变,故混合气体的密度不随时间变化而改变不能作为判断是否达到化学平衡状态的依据,故B错误;
C.NO2为红棕色气体,N2O4为无色气体,故混合气体的颜色不随时间变化而改变可作为判断是否达到化学平衡状态的依据,故C正确;
D.平均分子量=
,总质量不变,总物质的量在变,故反应混合气平均分子量不再改变可作为判断是否达到化学平衡状态的依据,故D正确,
故选B;
(2)由(1)可知,反应物为N2O4,生成物为NO2,反应进行到10min时,N2O4的物质的量变化为0.2mol/L×2L=0.4mol,共吸收热量22.76kJ,故反应1molN2O4共吸收热量22.76kJ×2.5=56.9kJ,故该反应热化学方程式为:N2O4(g)?2NO2(g)△H=+56.9kJ/mol;故答案为:N2O4(g)?2NO2(g)△H=+56.9kJ/mol;
(3)根据化学方程式N2O4(g)?2NO2(g),及平衡常数的定义可得k=
=
=0.9,故答案为:0.9;
(4)①恒容,充入一定量NO2,相当于增大压强,平衡逆向移动,新平衡后混合气体中NO2的体积分数减小,故W1>W2,故答案为:>;
②30min时,c(NO2)=0.9mol/L,k=
=
=0.9,c(N2O4)=0.9mol/L,
20min-30min,N2O4的浓度增加了0.9-0.4=0.5mol/L,故NO2的浓度减少了1mol/L,则20min时,c(NO2)=1+0.6=1.6mol/L,c(N2O4)=0.9mol/L,
故答案为: ;
;
Ⅱ、(1)放电时,该装置是原电池,Fe元素化合价由+3价变为+2价,得电子发生还原反应,所以该电极是正极,电极反应式为FePO4+e-+Li+=LiFePO4,
故答案为:正;FePO4+e-+Li+=LiFePO4;
(2)计算得到,电解含有0.01mol CuSO4和0.01molNaCl的混合溶液100mL,电路中转移了0.02mol e-,
阳极:2Cl--2e -=Cl2↑,
0.01mol 0.01mol 0.005mol
4OH--4e-=2H2O+O2↑,
0.01mol 0.01mol 0.0025mol
阴极:Cu2++2e-=Cu
0.01mol 0.02mol
所以阳极上生成的气体在标准状况下的体积=(0.005mol+0.0025mol)×22.4L/mol=0.168L,
故答案为:0.168.
B.密度=
| 总质量 |
| 体积 |
C.NO2为红棕色气体,N2O4为无色气体,故混合气体的颜色不随时间变化而改变可作为判断是否达到化学平衡状态的依据,故C正确;
D.平均分子量=
| 总质量 |
| 总物质的量 |
故选B;
(2)由(1)可知,反应物为N2O4,生成物为NO2,反应进行到10min时,N2O4的物质的量变化为0.2mol/L×2L=0.4mol,共吸收热量22.76kJ,故反应1molN2O4共吸收热量22.76kJ×2.5=56.9kJ,故该反应热化学方程式为:N2O4(g)?2NO2(g)△H=+56.9kJ/mol;故答案为:N2O4(g)?2NO2(g)△H=+56.9kJ/mol;
(3)根据化学方程式N2O4(g)?2NO2(g),及平衡常数的定义可得k=
| c2(NO2) |
| c(N2O4) |
| 0.6×0.6 |
| 0.4 |
(4)①恒容,充入一定量NO2,相当于增大压强,平衡逆向移动,新平衡后混合气体中NO2的体积分数减小,故W1>W2,故答案为:>;
②30min时,c(NO2)=0.9mol/L,k=
| c2(NO2) |
| c(N2O4) |
| 0.9×0.9 |
| c(N 2O4) |
20min-30min,N2O4的浓度增加了0.9-0.4=0.5mol/L,故NO2的浓度减少了1mol/L,则20min时,c(NO2)=1+0.6=1.6mol/L,c(N2O4)=0.9mol/L,
故答案为:
 ;
;Ⅱ、(1)放电时,该装置是原电池,Fe元素化合价由+3价变为+2价,得电子发生还原反应,所以该电极是正极,电极反应式为FePO4+e-+Li+=LiFePO4,
故答案为:正;FePO4+e-+Li+=LiFePO4;
(2)计算得到,电解含有0.01mol CuSO4和0.01molNaCl的混合溶液100mL,电路中转移了0.02mol e-,
阳极:2Cl--2e -=Cl2↑,
0.01mol 0.01mol 0.005mol
4OH--4e-=2H2O+O2↑,
0.01mol 0.01mol 0.0025mol
阴极:Cu2++2e-=Cu
0.01mol 0.02mol
所以阳极上生成的气体在标准状况下的体积=(0.005mol+0.0025mol)×22.4L/mol=0.168L,
故答案为:0.168.
点评:本题考查化学反应速率及化学平衡图象,化学电源新型电池,电解池原理的应用,注重对图象的分析,明确图象中纵横坐标及点、线、面的意义是解答本题的关键,要注意充分用好守恒的思想解决问题,难度中等.

练习册系列答案
相关题目
在恒温恒容条件下,一定能使反应A(g)+B(s)?C(g)+D(g)的反应速率增大的措施是( )
| A、减小A或B的用量 |
| B、减小C的量 |
| C、增大B的量 |
| D、增大D的量 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、7.8 g苯中含有0.3NA个碳碳双键,0.3NA个碳碳单键 |
| B、5.6 g铁与足量的稀硝酸反应,失去电子数为0.2NA |
C、 32g硫(结构见图)含S-S的数目为NA 32g硫(结构见图)含S-S的数目为NA |
| D、含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA |

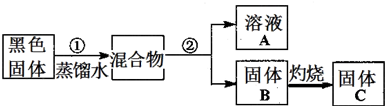
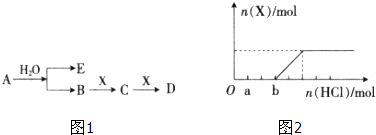
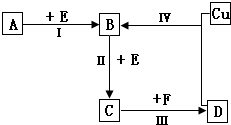 有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题: