题目内容
用铂电极电解M(NO3)x溶液,当阴极析出mg金属M时,在阳极放出560mL气体(标准状况),则金属M的相对原子质量为( )
| A、10mx | ||
B、
| ||
C、
| ||
D、
|
考点:电解原理
专题:电化学专题
分析:用石墨作电极电解M(NO3)x溶液,即+x价金属的硝酸盐溶液,两极反应分别为:阳极:4OH-=4e-+2H2O+O2↑,阴极:Mx++xe-=M,根据阳极产生气体的量可以计算转移电子数,根据电子守恒来计算金属的相对原子质量.
解答:
解:阳极电极反应:4OH-=4e-+2H2O+O2↑,当产生0.56L即0.025moL氧气,共发生0.1mol电子转移,在阴极是金属阳离子得电子生成金属的过程,由发生电极反应:Mx++xe-=M,再根据电子守恒,则转移0.1mol电子析出金属M的物质的量为
mol,设相对原子质量是M,则
?M=m,解得x=10mx.
故选A.
| 0.1 |
| x |
| 0.1 |
| x |
故选A.
点评:本题考查学生电化学的有关计算知识,注意电子守恒的灵活应用,属于基本知识的考查,难度不大.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
检验SO2气体中是否混有CO2气体,可采用的方法是( )
| A、通过品红溶液 |
| B、通过盐酸,再通过BaCl2溶液 |
| C、先通过NaOH溶液,再通过澄清石灰水 |
| D、先通过酸性KMnO4溶液,再通过澄清石灰水 |
将某些化学知识用数轴表示直观形象、简明易记.下列用数轴表示不正确的是( )
A、碳在氧气中燃烧,n(C)/n(O2)与生成物的关系: |
B、分散系的分类与分散质粒直径大小关系: |
C、AlCl3和NaOH反应后铝元素的存在形式与反应物中n(OH-)/n(Al3+) |
D、Na与O2反应的产物与反应物n(Na)/n(O2)的关系: |
某工厂用硫酸处理氨气尾气,得到铵盐(不同批次得到a、b、c三种不同的铵盐).称取不同质量的铵盐,加入到固定量的NaOH溶液中并加热,收集氨气,得到如下生成氨气的量与加入铵盐的量关系图:下列判断不正确的是( )
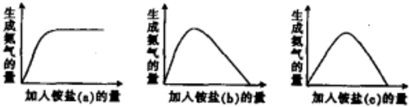

| A、a对应的铵盐是(NH4)2SO4 |
| B、b对应的铵盐是(NH4)2SO4和NH4HSO4 |
| C、c对应的铵盐是NH4HSO4 |
| D、当b和c铵盐的质量相同时,可得到相同量的氨气 |
标准状况下电解200mLNaCl、CuSO4的混合溶液,阴阳两极所得气体的体积随时间变化如图所示,则c(CuSO4)为( )
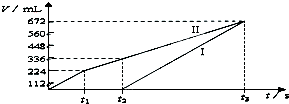

| A、0.1mol/L |
| B、0.15mol/L |
| C、0.2mol/L |
| D、0.25mol/L |
药物是人们生活的必备品之一,下列药物的主要成分都能发生以下四种反应的是( )
①取代反应②加成反应③水解反应④中和反应

①取代反应②加成反应③水解反应④中和反应

| A、维生素 | B、阿司匹林 |
| C、芬必得 | D、扑热息痛 |
实验室需配制一种仅含四种离子(不包括水电离出的离子)的混合溶液,且在混合液中四种离子的物质的量浓度均为0.5mol/L,下面四个选项中能达到此目的是( )
| A、Fe2+、Na+、NO3-、Cl- |
| B、Mg2+、NH4+、SO42-、NO3- |
| C、H+、K+、Cl-、CH3COO- |
| D、Fe3+、K+、AlO2-、SO42- |
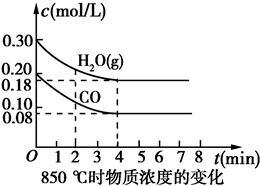 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示: