题目内容
某工厂用硫酸处理氨气尾气,得到铵盐(不同批次得到a、b、c三种不同的铵盐).称取不同质量的铵盐,加入到固定量的NaOH溶液中并加热,收集氨气,得到如下生成氨气的量与加入铵盐的量关系图:下列判断不正确的是( )
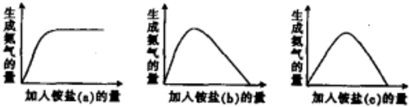

| A、a对应的铵盐是(NH4)2SO4 |
| B、b对应的铵盐是(NH4)2SO4和NH4HSO4 |
| C、c对应的铵盐是NH4HSO4 |
| D、当b和c铵盐的质量相同时,可得到相同量的氨气 |
考点:铵盐
专题:氮族元素
分析:根据酸碱中和的原理,可知存在反应的先后顺序:硫酸氢铵先和NaOH转化为硫酸铵,然后硫酸铵再和NaOH转化为氨气,因而第一个反应结束后剩余氢氧化钠的量决定第二个反应中生成氨气的多少,结合图中氨气与混合物质量之间关系解答.
解答:
解:根据酸碱中和的原理,可知存在反应的先后顺序:硫酸氢铵先和NaOH转化为硫酸铵,然后硫酸铵再和NaOH转化为氨气,因而第一个反应结束后剩余氢氧化钠的量决定第二个反应中生成氨气的多少,在氢氧化钠总量不变时,混合物的质量增多,硫酸氢铵增多,第一个反应后剩于氢氧化钠的量减少,第二个反应生成氨气必定减少.
A.氨气产生的量随着硫酸铵的加入先增加后不变,所以固体中只含有硫酸铵,故A正确;
B.混合物为(NH4)2SO4和NH4HSO4时,首先发生反应:2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O,然后才发生:(NH4)2SO4+2NaOH=2NH3↑+2Na2SO4+2H2O,在氢氧化钠总量不变时,混合物的质量增多,硫酸氢铵增多,第一个反应后剩于氢氧化钠的量减少,第二个反应生成氨气必定减少,故B正确;
C.混合物中只含NH4HSO4时,首先发生反应:2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O,然后才发生:(NH4)2SO4+2NaOH=2NH3↑+2Na2SO4+2H2O,依据硫酸氢铵消耗氢氧化钠的物质的量与硫酸铵消耗氢氧化钠的物质的量可知图象C符合题意,故C正确;
D.依据硫酸铵与硫酸氢铵与氢氧化钠反应的顺序可知,混合物中含有硫酸氢铵越多,与相同质量的氢氧化钠反应,生成的氨气越少,故D错误;
故选:D.
A.氨气产生的量随着硫酸铵的加入先增加后不变,所以固体中只含有硫酸铵,故A正确;
B.混合物为(NH4)2SO4和NH4HSO4时,首先发生反应:2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O,然后才发生:(NH4)2SO4+2NaOH=2NH3↑+2Na2SO4+2H2O,在氢氧化钠总量不变时,混合物的质量增多,硫酸氢铵增多,第一个反应后剩于氢氧化钠的量减少,第二个反应生成氨气必定减少,故B正确;
C.混合物中只含NH4HSO4时,首先发生反应:2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O,然后才发生:(NH4)2SO4+2NaOH=2NH3↑+2Na2SO4+2H2O,依据硫酸氢铵消耗氢氧化钠的物质的量与硫酸铵消耗氢氧化钠的物质的量可知图象C符合题意,故C正确;
D.依据硫酸铵与硫酸氢铵与氢氧化钠反应的顺序可知,混合物中含有硫酸氢铵越多,与相同质量的氢氧化钠反应,生成的氨气越少,故D错误;
故选:D.
点评:本题考查了铵盐性质,题目难度较大,侧重考查离子反应的先后顺序,明确氨根离子、氢离子与氢氧根离子反应的先后顺序是解题关键.

练习册系列答案
相关题目
柠檬烯醇是一种实用香精,其结构简式如图所示.下列有关柠檬烯醇的说法正确的是( )
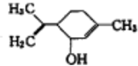

| A、能与氢氧化钠溶液发生中和反应 |
| B、能发生加成反应和取代反应 |
| C、不能使酸性高锰酸钾溶液褪色 |
D、与对丙基苯甲醇(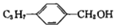 )互为同分异构体 )互为同分异构体 |
如今人们把食品分为绿色食品、蓝色食品、白色食品等类型.绿色植物通过光合作用转化的食品叫绿色食品;而直接从海洋获取的食品叫蓝色食品;可通过微生物发酵制得的食品叫白色食品.下面属于白色食品的( )
| A、乙醇 | B、面粉 | C、海带 | D、食盐 |
粗盐提纯实验的部分操作如图所示,其中错误的是( )
A、 取一定量的粗盐 |
B、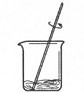 溶解 |
C、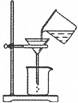 过滤 |
D、 蒸发 |
选择萃取剂将碘水中的碘萃取出来,这中萃取剂应具备的性质是( )
| A、不溶于水,且必须易与碘发生化学反应 |
| B、不溶于水,且比水更容易使碘溶解 |
| C、不溶于水,且密度必须比水大 |
| D、不溶于水,且密度必须比水小 |
用铂电极电解M(NO3)x溶液,当阴极析出mg金属M时,在阳极放出560mL气体(标准状况),则金属M的相对原子质量为( )
| A、10mx | ||
B、
| ||
C、
| ||
D、
|
把等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,经充分搅拌后,将所得溶液用石墨电极进行电解,阳极生成的物质是( )
| A、H2 |
| B、Ag |
| C、Cl2 |
| D、O2 |
下列溶液一定是碱性的是( )
| A、pH>7的某电解质的溶液 |
| B、c(OH-)>1×10-7mol/L |
| C、溶液中含有OH- |
| D、溶液中c(OH-)>c(H+) |
下列关于氯水的叙述正确的是( )
| A、新制氯水中只含Cl2和H2O分子 |
| B、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| C、氯水中存在次氯酸根,不存在次氯酸分子 |
| D、氯水放置数天后,pH将变大 |