题目内容
将某些化学知识用数轴表示直观形象、简明易记.下列用数轴表示不正确的是( )
A、碳在氧气中燃烧,n(C)/n(O2)与生成物的关系: |
B、分散系的分类与分散质粒直径大小关系: |
C、AlCl3和NaOH反应后铝元素的存在形式与反应物中n(OH-)/n(Al3+) |
D、Na与O2反应的产物与反应物n(Na)/n(O2)的关系: |
考点:钠的重要化合物,分散系、胶体与溶液的概念及关系,镁、铝的重要化合物
专题:溶液和胶体专题,几种重要的金属及其化合物
分析:A.碳和氧气反应可以生成一氧化碳、二氧化碳或混合物;
B.依据分散系的本质区别,分散质的直径大小分析判断;
C.依据氯化铝溶液中加入氢氧化钠溶液,随着加入的量增多,会先生成氢氧化铝沉淀,氢氧化铝沉淀溶解;
D.钠在不加热时与氧气反应生成氧化钠,加热反应生成过氧化钠.
B.依据分散系的本质区别,分散质的直径大小分析判断;
C.依据氯化铝溶液中加入氢氧化钠溶液,随着加入的量增多,会先生成氢氧化铝沉淀,氢氧化铝沉淀溶解;
D.钠在不加热时与氧气反应生成氧化钠,加热反应生成过氧化钠.
解答:
解:A.2C+CO2=2CO;C+O2=CO2;
≤1,产物为二氧化碳;
≥2,产物为一氧化碳;1<
<2,产物为一氧化碳和二氧化碳,故A正确;
B.溶液分散质直径<1nm,浊液分散质直径>100nm,胶体分散质直径在1nm-100nm,故B正确;
C.Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O,
<3,铝元素以Al3+和Al(OH)3形式存在;
=3,则以Al(OH)3形式存在;3<
<4以 AlO2-和Al(OH)3形式存在;
≥4只以 AlO2-形式存在,故C正确;
D.钠在空气中加热反应生成的是过氧化钠,发生2Na+O2
Na2O2,故D错误;
故选D.
| n(C) |
| n(o2) |
| n(C) |
| n(o2) |
| n(C) |
| n(o2) |
B.溶液分散质直径<1nm,浊液分散质直径>100nm,胶体分散质直径在1nm-100nm,故B正确;
C.Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O,
| n(NaOH) |
| n(AlCl3) |
| n(NaOH) |
| n(AlCl3) |
| n(NaOH) |
| n(AlCl3) |
| n(NaOH) |
| n(AlCl3) |
D.钠在空气中加热反应生成的是过氧化钠,发生2Na+O2
| ||
故选D.
点评:本题综合考查元素化合物知识,侧重于学生的分析能力的考查,是近年以来出现的一道很少出现的试题题型题,是一道新情景试题,具有很强的综合性,也具有极强的迷惑性,各选项具有很强的干扰性,是一道好题!很容易选错答案.主要考查学生对元素化合物知识的掌握情况.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
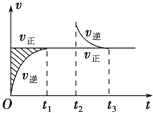 恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件.下列有关说法中正确的是( )
恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件.下列有关说法中正确的是( )| A、Z和W在该条件下都不可能为气态 |
| B、t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C、若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
| D、若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等. |
在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子.则该硫酸盐的物质的量浓度为( )
| A、2 mol?L-1 |
| B、2.5 mol?L-1 |
| C、5 mol?L-1 |
| D、7.5 mol?L-1 |
欲除去氯气中的少量氯化氢气体,最好选用( )
| A、H2O |
| B、NaOH |
| C、饱和食盐水 |
| D、石灰水 |
粗盐提纯实验的部分操作如图所示,其中错误的是( )
A、 取一定量的粗盐 |
B、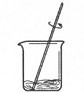 溶解 |
C、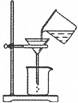 过滤 |
D、 蒸发 |
用铂电极电解M(NO3)x溶液,当阴极析出mg金属M时,在阳极放出560mL气体(标准状况),则金属M的相对原子质量为( )
| A、10mx | ||
B、
| ||
C、
| ||
D、
|
SiO2是一种化工原料,可以制备一系列物质(如图所示).下列说法错误的是( )
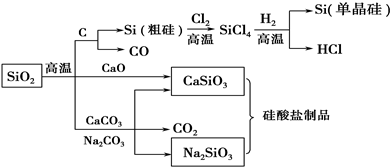

| A、高炉炼铁时,加入石灰石将铁矿石中的脉石(主要成分为SiO2)转化为易熔的炉渣 |
| B、纯净的二氧化硅和单晶硅都是信息产业的重要基础材料 |
| C、用盐酸可除去石英砂(主要成分为SiO2)中少量的碳酸钙 |
| D、图中所含反应都不属于氧化还原反应 |