题目内容
某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写) .
(2)实验中眼睛注视 ,直至滴定终点.判断到达终点的现象是 .
(3)滴定前平视KOH液面,刻度为 am L,滴定后俯视液面刻度为bmL,则(b-a)mL比实际消耗KOH溶液体积 (填“多”或“少”).根据(b-a)mL计算得到的待测浓度,比实际 填“大”或“小”).
(4)若酸式滴定管没有用盐酸润洗,对测定结果有何影响 (填“偏大”、“偏小”或“无影响”,其他操作均正确).
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)
(2)实验中眼睛注视
(3)滴定前平视KOH液面,刻度为 am L,滴定后俯视液面刻度为bmL,则(b-a)mL比实际消耗KOH溶液体积
(4)若酸式滴定管没有用盐酸润洗,对测定结果有何影响
考点:中和滴定
专题:实验题
分析:(1)根据中和滴定有检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等操作;
(2)实验中应控制流速并观察锥形瓶中颜色变化;如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)滴定后俯视液面刻度,则读数偏小,则(b-a)mL比实际消耗KOH溶液体积少;由c(待测)=
分析误差
(4)若酸式滴定管没有用盐酸润洗,盐酸的浓度变小,反应消耗标准液的体积偏小,根据c(待测)=
分析误差.
(2)实验中应控制流速并观察锥形瓶中颜色变化;如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)滴定后俯视液面刻度,则读数偏小,则(b-a)mL比实际消耗KOH溶液体积少;由c(待测)=
| c(标准)×V(标准) |
| V(待测) |
(4)若酸式滴定管没有用盐酸润洗,盐酸的浓度变小,反应消耗标准液的体积偏小,根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
解答:
解:(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,则正确的顺序为BDCEAF,
故答案为:BDCEAF;
(2)滴定时,滴定过程中,用左手控制碱式滴定管橡皮管玻璃珠处,右手摇动锥形瓶,两眼应该注视锥形瓶内溶液的颜色变化;滴定时,锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色,可说明达到滴定终点;
故答案为:锥形瓶中溶液的颜色变化;锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色;
(3)滴定前平视KOH液面,刻度为aml,滴定后俯视液面刻度为bmL,则滴定后读数偏小,则(b-a)mL比实际消耗KOH溶液体积少;由c(待测)=
可知计算得到的盐酸的浓度偏小;
故答案为:少;小;
(4)若酸式滴定管没有用盐酸润洗,盐酸的浓度变小,滴定时反应消耗标准液的体积偏小,根据c(待测)=
可知,计算结果偏小;
故答案为:偏小.
故答案为:BDCEAF;
(2)滴定时,滴定过程中,用左手控制碱式滴定管橡皮管玻璃珠处,右手摇动锥形瓶,两眼应该注视锥形瓶内溶液的颜色变化;滴定时,锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色,可说明达到滴定终点;
故答案为:锥形瓶中溶液的颜色变化;锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色;
(3)滴定前平视KOH液面,刻度为aml,滴定后俯视液面刻度为bmL,则滴定后读数偏小,则(b-a)mL比实际消耗KOH溶液体积少;由c(待测)=
| c(标准)×V(标准) |
| V(待测) |
故答案为:少;小;
(4)若酸式滴定管没有用盐酸润洗,盐酸的浓度变小,滴定时反应消耗标准液的体积偏小,根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
故答案为:偏小.
点评:本题考查酸碱中和滴定实验,题目难度不大,注意把握实验的步骤、方法以及注意事项,在误差分析时根据c(待测)=
分析即可.
| c(标准)×V(标准) |
| V(待测) |

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
能再溶液中大量共存的一组离子是( )
| A、Na+、Ba2+、OH-、NO3- |
| B、Al3+、NH4+、OH-、Cl- |
| C、K+、Na+、ClO-、SO32- |
| D、H+、Na+、AlO2-、Cl- |
下列有关实验操作正确的是( )
A、 |
B、 |
C、 |
D、 |
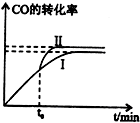 二甲醚是一种重要的清洁燃料,有多种合成方法.
二甲醚是一种重要的清洁燃料,有多种合成方法.
 的邻位异构体分子内脱水产物,香豆素的结构简式为
的邻位异构体分子内脱水产物,香豆素的结构简式为
 在一定条件下可水解为
在一定条件下可水解为 ;则F
;则F 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.