题目内容
向mg镁和铝的混合物重加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL.向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng.再将得到的沉淀灼烧至质量不再改变为止,得到固体pg.则下列关系不正确的是( )
A、c=
| ||||
B、p=m+
| ||||
| C、n=m+17Vc | ||||
D、
|
考点:有关混合物反应的计算
专题:计算题
分析:反应化学方程式为:Mg+H2SO4=MgSO4+H2↑;2Al+3H2SO4=Al2(SO4)3+3H2↑;MgSO4+2KOH=Mg(OH)2↓+K2SO4;Al2(SO4)3+6KOH=2Al(OH)3↓+3K2SO4;Mg(OH)2
MgO+H2O;2Al(OH)3
Al2O3+3H2O;
A.根据n=
计算氢气的物质的量,根据电荷守恒,氢氧化镁、氢氧化铝沉淀中含有n(OH-)等于金属提供的电子的物质的量,等于生成氢气的获得的电子的物质的量,据此计算氢氧根离子的物质的量,再根据c=
计算氢氧化钾的物质的量浓度;
B.由Mg(OH)2
MgO+H2O,2Al(OH)3
Al2O3+3H2O可知,沉淀灼烧生成氧化镁与氧化铝,二者质量等于金属质量与氧原子的质量之和,由方程式可知氧原子的物质的量等于氢氧根离子物质的量的一半,据此计算;
C.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,根据n=cVM计算氢氧根离子的质量;
D.按照极值方法计算,若mg全是镁,计算生成得到的氧化镁质量,若mg全是铝,计算得到的氧化铝的质量,实际固体的质量介于二者之间.
| ||
| ||
A.根据n=
| V |
| Vm |
| n |
| V |
B.由Mg(OH)2
| ||
| ||
C.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,根据n=cVM计算氢氧根离子的质量;
D.按照极值方法计算,若mg全是镁,计算生成得到的氧化镁质量,若mg全是铝,计算得到的氧化铝的质量,实际固体的质量介于二者之间.
解答:
解:A.根据电荷守恒,氢氧化镁、氢氧化铝沉淀中含有n(OH-),等于金属提供的电子的物质的量,等于生成氢气的获得的电子的物质的量,故生成的氢气的物质的量等于参加反应的碱的物质的量的一半,故
×2=cmol/L×V×10-3L,整理得c=
,故A正确;
B.选项中p为生成的氧化物的质量,由Mg(OH)2
MgO+H2O,2Al(OH)3
Al2O3+3H2O可知,氧化物的质量等于金属质量与氧原子的质量之和,由方程式可知氧原子的物质的量等于氢氧根离子物质的量的一半,故p=m+c×V×10-3×
×16=m+
,故B正确;
C.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,故n=m+c×V×10-3×17=m+
,故C错误;
D.得到的氧化物为氧化镁,根据元素守恒,则质量为P=
×40=
,若mg全是铝,得到的氧化物为氧化铝,根据元素守恒,则质量为p=
×
×102=
,质量介于二者之间,故D正确;
故选C.
| bL |
| 22.4L/mol |
| 1000b |
| 11.2V |
B.选项中p为生成的氧化物的质量,由Mg(OH)2
| ||
| ||
| 1 |
| 2 |
| cV |
| 125 |
C.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,故n=m+c×V×10-3×17=m+
| 17Vc |
| 1000 |
D.得到的氧化物为氧化镁,根据元素守恒,则质量为P=
| m |
| 24 |
| 5m |
| 3 |
| m |
| 27 |
| 1 |
| 2 |
| 17m |
| 9 |
故选C.
点评:本题综合考查镁铝元素单质及化合物的性质、混合物的有关计算,注意利用方程式与电子转移守恒寻找关系解答,题目计算量较大,且为无数据计算,难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
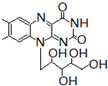 核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构如图所示:已知:
核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构如图所示:已知: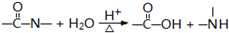
有关核黄素的下列说法中,不正确的是( )
| A、该化合物的分子式为C17H22N4O6 |
| B、酸性条件下加热水解,有CO2生成 |
| C、该分子中有3个手性碳原子(与4个不同基团连接的碳原子叫手性碳原子) |
| D、能发生酯化反应 |
微量元素是指含量在人体总重量的0.01%以下的元素,这些元素对人体的正常发育和健康起着主要作用,下列各组元素全部是微量元素的是( )
| A、Na、K、Cl、S、O |
| B、N、H、O、P、C |
| C、F、I、Fe、Zn、Cu |
| D、Ge、Se、Cu、Mg、C |
现有常温下的四种溶液(如下表),下列有关叙述中正确的是( )
| ① | ② | ③ | ④ | |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A、在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 |
| B、温度下降10℃,四种溶液的pH均不变 |
| C、分别加水稀释10倍,四种溶液的pH:①>②>③>④ |
| D、将①、④两种溶液等体积混合,所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
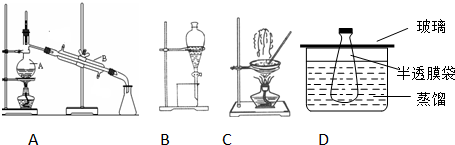

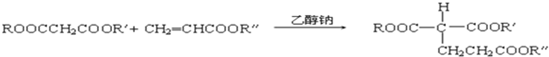 (R、R′、R″代表相同或不相同的烃基).
(R、R′、R″代表相同或不相同的烃基).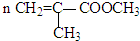
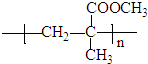
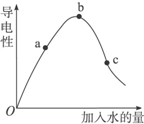 一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示.请完成下列问题:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示.请完成下列问题: