题目内容
8.联氨(N2H4)是一种应用广泛的化工原料,可用作火箭燃料.已知:①N2H4(l)+$\frac{1}{2}$N2O4(l)═$\frac{3}{2}$N2(g)+2H2O(l)△H=-546.45kJ/mol
②H2O(g)═H2O(l)△H=-44.0kJ/mol
则2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g) 的△H是( )
| A. | -916.9 kJ/mol | B. | -458.45 kJ/mol | C. | +916.9 kJ/mol | D. | +458.45 kJ/mol |
分析 由①N2H4(l)+$\frac{1}{2}$N2O4(l)═$\frac{3}{2}$N2(g)+2H2O(l)△H=-546.45kJ/mol
②H2O(g)═H2O(l)△H=-44.0kJ/mol
结合盖斯定律可知①×2-②×4得到2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g),以此来解答.
解答 解:由①N2H4(l)+$\frac{1}{2}$N2O4(l)═$\frac{3}{2}$N2(g)+2H2O(l)△H=-546.45kJ/mol
②H2O(g)═H2O(l)△H=-44.0kJ/mol
结合盖斯定律可知①×2-②×4得到2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g),其△H=(-546.45kJ/mol)×2-(-44kJ/mol)×4=-916.9 kJ/mol,
故选A.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、盖斯定律的应用为解答的关键,侧重分析与应用能力的考查,注意反应的关系,题目难度不大.

练习册系列答案
相关题目
19.100mL 2.0 mol•L-1 的碳酸钠溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,最终都有气体产生,但生成的气体体积不同,下列选项中盐酸的浓度合理的是( )
| A. | 2.0 mol•L-1 | B. | 1.5 mol•L-1 | C. | 1 mol•L-1 | D. | 0.5 mol•L-1 |
16.将 25℃,100mL 0.1mol/L 下列物质的水溶液加热至 80℃(溶液体积变化忽略不计),溶液的 pH 保 持不变的是( )
| A. | H2SO4 | B. | CH3COOH | C. | (NH4)2 SO4 | D. | NaOH |
3.如图是利用废铜屑(含杂质)制备胆矾(硫酸铜晶体)的过程
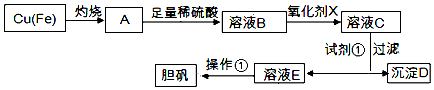
已知:
请回答:
(1)下列物质中最适宜做氧化剂X的是B(填字母).
A.NaClO B.H2O2 C.KMnO4 D.FeCl3
(2)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(3)操作①的名称是蒸发浓缩、冷却结晶.
(4)沉淀D加入盐酸可以得到FeCl3溶液,关于FeCl3溶液的性质中说法不正确的是C.
A.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
C.将FeCl3溶液滴加NaOH溶液,将沉淀干燥灼烧,得到Fe(OH)3固体
D.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,其原因是Fe+2Fe3+=3Fe2+(用离子方程式表示).
(6)若用碳电极电解硫酸铜溶液200mL.通电5min后,阴极增重0.64g,则电解后溶液的pH=1(溶液体积变化忽略不计).

已知:
| 溶液中被沉淀的离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物的沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
(1)下列物质中最适宜做氧化剂X的是B(填字母).
A.NaClO B.H2O2 C.KMnO4 D.FeCl3
(2)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(3)操作①的名称是蒸发浓缩、冷却结晶.
(4)沉淀D加入盐酸可以得到FeCl3溶液,关于FeCl3溶液的性质中说法不正确的是C.
A.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
C.将FeCl3溶液滴加NaOH溶液,将沉淀干燥灼烧,得到Fe(OH)3固体
D.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,其原因是Fe+2Fe3+=3Fe2+(用离子方程式表示).
(6)若用碳电极电解硫酸铜溶液200mL.通电5min后,阴极增重0.64g,则电解后溶液的pH=1(溶液体积变化忽略不计).
20.制备干燥的氨气所需的药品是( )
| A. | NH4Cl溶液、NaOH溶液、碱石灰 | B. | 浓氨水、NaOH固体、浓硫酸 | ||
| C. | NH4Cl固体、消石灰、碱石灰 | D. | 浓NaOH溶液、NH4C固体、浓硫酸 |
17.下列实验操作或装置正确的是( )

| A. | ①分离出BaSO4浊液中的BaSO4 | |
| B. | ②除去CO2中少量HCl气体 | |
| C. | ③配制一定物质的量浓度溶液时转移溶液 | |
| D. | ④制取一定量的CO2 |