题目内容
甲、乙两种常见的烃各7.8g,完全燃烧后生成的气体分别通入足量的石灰水中,均能得到60g沉淀.在同温同压下,同体积甲的质量是H2质量的13倍,相同条件下甲与乙的蒸汽密度比为1:3,试通过计算确定甲与乙的结构简式.
考点:有机物实验式和分子式的确定
专题:烃及其衍生物的燃烧规律
分析:通入足量石灰水生成的沉淀为碳酸钙,根据碳酸钙的质量可以计算出碳酸钙的物质的量,根据C原子守恒计算出甲中含有的C原子数,测得在同温、同压、同体积时甲的质量是H2质量的13倍,根据m=nM可知,该甲的摩尔质量为氢气的13倍,据此可以计算出甲的摩尔质量,相同条件下甲与乙的蒸汽密度比等于其摩尔质量之比,可知乙的摩尔质量为甲的摩尔质量的3倍,然后计算出7.8g甲的物质的量,根据摩尔质量计算出分子式,根据分子式确定结构简式.
解答:
解:7.8该烃完全燃烧后生成的气体通入足量的石灰水,得到60克沉淀,沉淀为碳酸钙,其物质的量为:
=0.6mol,根据质量守恒,7.8g该烃中含有C的物质的量为0.6mol;
在同温、同压、同体积的气体具有相同的物质的量,根据m=nM可知,甲的摩尔质量是H2质量的13倍,甲的摩尔质量为:2g/mol×13=26g/mol,
7.8g甲的物质的量为:n=
=0.3mol,
甲中含有碳原子数为:
=2,
则甲分子中含有H的数目为:
=2,
该甲的分子式为:C2H2,为乙炔,其结构简式为:CH≡CH,
相同条件下甲与乙的蒸汽密度比等于其摩尔质量之比,可知乙的摩尔质量为甲的摩尔质量的3倍,则乙的摩尔质量为26g/mol×3=78g/mol,
7.8g乙的物质的量为
=0.1mol,
乙中含有碳原子数为
=6,
则乙中所含H的数目为
=6,
则乙的分子式为C6H6,常见的烃为苯,结构简式为: ,
,
答:甲的结构简式为CH≡CH,乙的结构简式为 .
.
| 60g |
| 100g/mol |
在同温、同压、同体积的气体具有相同的物质的量,根据m=nM可知,甲的摩尔质量是H2质量的13倍,甲的摩尔质量为:2g/mol×13=26g/mol,
7.8g甲的物质的量为:n=
| 7.8g |
| 26g/mol |
甲中含有碳原子数为:
| 0.6mol |
| 0.3mol |
则甲分子中含有H的数目为:
| 26-12×2 |
| 1 |
该甲的分子式为:C2H2,为乙炔,其结构简式为:CH≡CH,
相同条件下甲与乙的蒸汽密度比等于其摩尔质量之比,可知乙的摩尔质量为甲的摩尔质量的3倍,则乙的摩尔质量为26g/mol×3=78g/mol,
7.8g乙的物质的量为
| 7.8g |
| 78g/mol |
乙中含有碳原子数为
| 0.6mol |
| 0.1mol |
则乙中所含H的数目为
| 78-12×6 |
| 1 |
则乙的分子式为C6H6,常见的烃为苯,结构简式为:
 ,
,答:甲的结构简式为CH≡CH,乙的结构简式为
 .
.
点评:本题考查了有机物分子式、结构简式的确定,题目难度不大,注意掌握常见有机物结构与性质,能够根据质量守恒、烃的燃烧通式计算有机物的分子式、结构简式,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
地壳中含量第一和第二的两种元素所形成的化合物不具有的性质是( )
| A、熔点很高 |
| B、与水反应生成对应的酸 |
| C、可与烧碱反应生成盐 |
| D、坚硬 |
 1mol C6H6与H2加成时:Ⅰ需
1mol C6H6与H2加成时:Ⅰ需 立体结构:该结构的二氯代物有
立体结构:该结构的二氯代物有 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯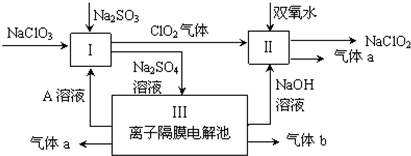
 四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃,拟利用图中的仪器,设计组装一套实验装置,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热).请回答下列各问题.
四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃,拟利用图中的仪器,设计组装一套实验装置,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热).请回答下列各问题.