题目内容
11.X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的2倍,Y元素在地壳中含量最多,Z元素金属性最强,R原子的核外电子数是X、Z核外电子数之和.下列叙述一定正确的是( )| A. | 氢化物的沸点Y>R>X | B. | 含氧酸酸性R>X | ||
| C. | X、Y不可能共存于离子化合物中 | D. | 原子半径Z>R>X>Y |
分析 X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的2倍,原子只能有2个电子层,最外层电子数为4,故X为C;Y元素在地壳中含量最多,则Y为O;Z元素金属性最强,则Z为Na;R原子的核外电子数是X、Z核外电子数之和,R原子核外电子数为6+11=17,故R为Cl.
解答 解:X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的2倍,原子只能有2个电子层,最外层电子数为4,故X为C;Y元素在地壳中含量最多,则Y为O;Z元素金属性最强,则Z为Na;R原子的核外电子数是X、Z核外电子数之和,R原子核外电子数为6+11=17,故R为Cl.
A.碳元素形成的氢化物为烃,有气体、液体、固体,故碳元素氢化物沸点不一定最小,故A错误;
B.碳酸的酸性比HClO的酸性强,故B错误;
C.C、O可能共存于离子化合物中,如碳酸钠等,故C错误;
D.同周期自左而右原子半径减小,一般电子层越多原子半径越大,故原子半径Z(Na)>R(Cl)>X(C)>Y(O),故D正确,
故选:D.
点评 本题考查结构性质位置关系应用,A、B选项为易错点,A选项中学生容易考虑甲烷,而忽略烃类物质,B选项学生容易根据最高价含氧酸酸性判断.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
1.短周期主族元素A、B、C、D、E的原子序数依次递增,A的单质在常温下呈气态,D元素的单质既能与盐酸反应也能与NaOH溶液反应,B、C、E原子的最外层电子数之和为13,E原子的最外层电子数是B原子内层电子数的3倍或是C原子最外层电子数的3倍.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(B)<r(C)<r(D) | |
| B. | 元素B、E的最高价氧化物的水化物都是强酸 | |
| C. | C、D的氧化物都能与氢氧化钠反应 | |
| D. | 工业上常用电解元素C、D的氯化物来制取它们的单质 |
2.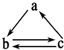 下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
 下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )| 物质 选项 | a | b | c |
| A | SiO2 | Na2SiO3 | H2SiO3 |
| B | C | CO | CO2 |
| C | Fe | FeCl2 | FeCl3 |
| D | CuO | Cu(OH)2 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
19.原子序数依次递增的4种短周期元素可形成简单离子,W2-、X+、Y3+、Z2-下列说法不正确的是( )
| A. | 离子半径由大到小:Z2->X+>Y3+>W2- | |
| B. | 气态氢化物的稳定性:H2W强于H2Z | |
| C. | 工业上常采用电解法冶炼Y 单质 | |
| D. | W、X 形成的化合物中阴、阳离子个数比一定是1:2 |
6.下列对晶体类型判断正确的是( )
| 选项 | Na2B2O7 | CaF2 | H3BO3 | NH3 |
| A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
| B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
| C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
| D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |
| A. | A | B. | B | C. | C | D. | D |
3.化学用语是学习化学的重要工具.下列用来表示物质变化的化学用语正确的是( )
| A. | 氢氧燃料电池的正极反应式为H2+2OH--2e-═2H2O | |
| B. | 用铂电极电解硫酸铜溶液的阳极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 表示醋酸与NaOH的稀溶液反应的中和热的化学方程式为H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ.mol-1 | |
| D. | NaHSO3溶于水时水解的离子方程式为HSO3-+H2O?SO32-+H3O+ |
20.在MgSO4和Al2(SO4)3的混合溶液中,c(Al3+)=0.4mol•L-1,c(SO42-)=0.9mol•L-1,则c(Mg2+)为( )
| A. | 0.5 mol•L-1 | B. | 0.4 mol•L-1 | C. | 0.3 mol•L-1 | D. | 0.2 mol•L-1 |
1.下列关于氯气、钠、镁的说法中,正确的是( )
| A. | 镁条燃烧可用泡沫灭火器灭火 | |
| B. | 工业上电解氯化钠、氯化镁溶液制取可以得到金属钠、镁 | |
| C. | 通常情况下,铁是银白色金属,硬度较大,可以被磁石吸引 | |
| D. | 铜能与氯化铁溶液反应,该反应可以用于印刷电路板的制作 |