题目内容
10.在强碱的无色溶液中,下列各组离子能大量共存的是( )| A. | K+、Na+、NO3-、Br- | B. | Na+、NH4+、NO3-、Cl- | ||
| C. | K+、Na+、HCO3-、NO3- | D. | K+、Cu2+、Cl-、SO42- |
分析 无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,强碱性溶液中存在大量氢氧根离子,
A.四种离子之间不反应,都不与氢氧根离子反应,且都是无色离子;
B.铵根离子与氢氧根离子反应;
C.碳酸氢根离子与氢氧根离子反应;
D.铜离子为有色离子,且铜离子与氢氧根离子反应.
解答 解:强碱性溶液中存在大量氢氧根离子,无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.K+、Na+、NO3-、Br-之间不反应,都不与氢氧根离子反应,且为无色溶液,在溶液中能够大量共存,故A正确;
B.NH4+与氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.HCO3-与氢氧根离子反应,在溶液中不能大量共存,故C错误;
D.Cu2+为有色离子,不满足溶液无色的条件,且Cu2+与氢氧根离子反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
20.下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是( )
①NH4HCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3.
①NH4HCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3.
| A. | ②③④ | B. | ②③④⑤ | C. | ①②③④ | D. | 全部 |
1.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):H2(g)+Cl2(g)→2HCl(g)+Q1 ①; H2(g)+Br2(g)→2HBr(g)+Q2②有关上述反应的叙述错误的是( )
| A. | Ql>Q2 | |
| B. | 反应物总能量均高于生成物总能量 | |
| C. | 1molHBr(g)具有的能量大于1molHBr(l)具有的能量 | |
| D. | 反应①生成2 molHCl(l)时放出Q1热量 |
18.一定温度压强下,O2与CH4的混合物密度是氢气的10倍,则 O2与CH4的物质的量之比为( )
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 1:3 |
5.每到冬天就会出现大雾天气,能见度不到10米,致使汽车行驶受阻,下列关于雾的说法正确的是( )
| A. | 无法确定雾中水滴的直径大小 | B. | 不会产生丁达尔现象 | ||
| C. | 雾中水滴的直径在1nm~100nm间 | D. | 雾中水滴的直径小于1nm |
15.已知 Na2SO4和 NaCl 混合溶液中,Cl-的物质的量浓度是 Na+的物质的量浓度的 $\frac{3}{5}$ 倍,下列叙 述中正确的是( )
| A. | Na2SO4和 NaCl 的物质的量之比为 1:3 | |
| B. | 溶液中一定有 1molNa2SO4 和 3molNaCl | |
| C. | 所带电荷数 SO42-是 Na+的 $\frac{3}{5}$ 倍 | |
| D. | SO42-与 Cl-的物质的量之和等于 Na+的物质的量 |
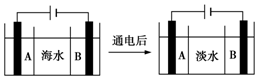 水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.
水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.