题目内容
12.已知A是石油裂解产物之一,对氢气的相对密度为14,D是含有7个碳原子的芳香族化合物.物质间的相互转化关系如图所示:
已知:RX$→_{△}^{NaOH/H_{2}O}$ROH
(1)A中含有的官能团名称为碳碳双键.
(2)写出E的结构简式
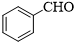 .
.(3)写出C+F→G的化学方程式
 .
.(4)关于化合物D,下列说法正确的是①③④.
①能与H2发生加成反应 ②能使Br2/CCl4溶液褪色
③与活泼金属反应 ④能与浓硝酸发生取代反应
(5)分子式为C8H8O2且与F互为同系物的同分异构体有4种.
分析 A是石油裂解产物之一,对氢气的相对密度为14,A的相对分子质量为28,则A为CH2=CH2,与溴发生加成反生成B为BrCH2CH2Br,B发生水解反应生成C为HOCH2CH2OH,D是含有7个碳原子的芳香族化合物,能连续发生氧化反应,则D为 ,E为
,E为 ,F为
,F为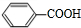 ,F与C发生酯化反应生成G,结构G的分子式可知,G的结构简式为:
,F与C发生酯化反应生成G,结构G的分子式可知,G的结构简式为: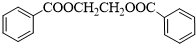 .
.
解答 解:A是石油裂解产物之一,对氢气的相对密度为14,A的相对分子质量为28,则A为CH2=CH2,与溴发生加成反生成B为BrCH2CH2Br,B发生水解反应生成C为HOCH2CH2OH,D是含有7个碳原子的芳香族化合物,能连续发生氧化反应,则D为 ,E为
,E为 ,F为
,F为 ,F与C发生酯化反应生成G,结构G的分子式可知,G的结构简式为:
,F与C发生酯化反应生成G,结构G的分子式可知,G的结构简式为: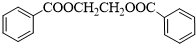 .
.
(1)A为CH2=CH2,含有的官能团名称为:碳碳双键,故答案为:碳碳双键;
(2)E的结构简式为 ,故答案为:
,故答案为: ;
;
(3)C+F→G的化学方程式: ,
,
故答案为: ;
;
(4)化合物D为 ,
,
①含有苯环,能与H2发生加成反应,故正确;
②苯环不能使Br2/CCl4溶液褪色,故错误;
③含有羟基,能与活泼金属反应,故正确;
④含有苯环,能与浓硝酸发生取代反应,故正确,
故选:①③④;
(5)分子式为C8H8O2且与F( )互为同系物的同分异构体,可以是苯乙酸,也可以是甲基苯甲酸,有邻、间、对三种,共有4种,
)互为同系物的同分异构体,可以是苯乙酸,也可以是甲基苯甲酸,有邻、间、对三种,共有4种,
故答案为:4.
点评 本题考查有机物的推断,充分利用反应条件进行推断,需要学生熟练掌握官能团的性质与转化,是对有机化学基础的综合考查.

练习册系列答案
相关题目
2.一定量的Fe和Fe2O3的混合物投入250ml密度为1.065g.cm-3、物质的量浓度为2mol•L-1的HNO3溶液中,固体恰好完全溶解,生成Fe(NO3)2和1.12LNO(标况下,且假定HNO3还原产物仅此一种).向反应后的溶液中加入1mol•L-1NaOH溶液,使铁元素完全沉淀下来,下列说法正确的是( )
| A. | 混合物中含有0.05molFe元素 | |
| B. | 该硝酸溶液中溶质的质量分数是63% | |
| C. | 所加入NaOH溶液的体积最少是450mL | |
| D. | 反应中HNO3被氧化,生成氧化产物NO |
7.X、Y、Z、W、M为原子序数依次增大的短周期主族元素.已知:
①元素对应的原子半径大小为:X<Z<Y<M<W;
②Y是组成有机物的必要元素
③Z与X可形成两种常见的共价化合物,与W可形成两种常见的离子化合物;
④M的电子层数与最外层电子数相等.
下列说法不正确的是( )
①元素对应的原子半径大小为:X<Z<Y<M<W;
②Y是组成有机物的必要元素
③Z与X可形成两种常见的共价化合物,与W可形成两种常见的离子化合物;
④M的电子层数与最外层电子数相等.
下列说法不正确的是( )
| A. | W、M的离子半径及最高价氧化物对应水化物的碱性皆为M<W | |
| B. | YZ2为直线型的共价化合物,W2Z2既含有离子键又含有共价键 | |
| C. | Y与X形成的化合物的熔沸点一定低于Z与X形成的化合物的熔沸点 | |
| D. | Z与M形成的化合物可作为耐高温材料,W、M、X以1:1:4组成的化合物是应用前景很广泛的储氢材料,具有很强的还原性 |
17.下列有关实验的描述不正确的是( )
| A. | 钠在空气和氯气中燃烧,火焰皆呈黄色,但生成固体颜色不同 | |
| B. | 新制饱和氯水和浓硝酸光照下会有气体产生,其成分中有氧气 | |
| C. | 次氯酸和过氧化钠都能使品红溶液褪色,其原理是不相同的 | |
| D. | 灼烧NaOH固体时不能使用瓷坩埚,因为坩埚中的SiO2能与NaOH反应 |
1.合成氨反应为N2+3H2?2NH3,今有A、B、C、D四个容器,每个容器中有两种操作,两种操作分别达到平衡后,操作1中N2和操作2中NH3转化率之和一定不为1的是(起始体积相等)( )
| A. | 恒温恒容:操作1:加1 mol N2+3 molH2,操作2:加2 mol NH3 | |
| B. | 恒温恒压:操作1:加1 mol N2+3 molH2,操作2:加2 mol NH3 | |
| C. | 恒温恒容:操作1:加1 mol N2+3 molH2,操作2:加3 mol NH3 | |
| D. | 恒温恒压:操作1:加1 mol N2+3 molH2,操作2:加3 mol NH3 |
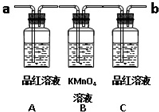 已知二氧化硫可使高锰酸钾溶液褪色,用如图装置(部分装置没画出)来验证某混合气体中同时含有SO2和CO2.
已知二氧化硫可使高锰酸钾溶液褪色,用如图装置(部分装置没画出)来验证某混合气体中同时含有SO2和CO2.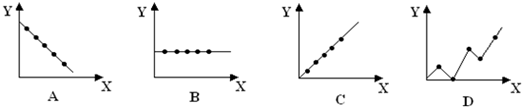
 .
.