题目内容
3.某反应体系的物质有H2SO4、Cu2O、Fe2(SO4)3、CuSO4、FeSO4、H2O.(1)请将Cu2O之外反应物与生成物分别填入横线内并配平.
Cu2O+Fe2(SO4)3+H2SO4→2CuSO4+2FeSO4+H2O
(2)反应中,被还原的元素是Fe,还原剂是Cu2O.
(3)每1molCu2O完全反应,转移的电子数目为2NA或12.04×1023.
分析 由题给物质可知,Cu2O为反应物,反应生成CuSO4,Cu元素化合价由+1价升高到+2,被氧化,反应中元素化合价变化的还有Fe元素,则氧化剂应为Fe2(SO4)3,FeSO4为还原产物,结合元素化合价变化解答该题.
解答 解:(1)由题给物质可知,Cu2O为反应物,反应生成CuSO4,Cu元素化合价由+1价升高到+2,被氧化,反应中元素化合价变化的还有Fe元素,则氧化剂应为Fe2(SO4)3,FeSO4为还原产物,Fe元素化合价由+3价降低到+2价,反应的方程式为Cu2O+Fe2(SO4)3+H2SO4═2CuSO4+2FeSO4+H2O,
故答案为:Cu2O;Fe2(SO4)3;H2SO4;2CuSO4;2FeSO4;H2O;
(2)Fe元素化合价由+3价降低到+2价,被还原,Cu元素化合价由+1价升高到+2价,为被氧化,Cu2O为还原剂,故答案为:Fe; Cu2O;
(3)Cu元素化合价由+1价升高到+2价,每1molCu2O完全反应,则失去2mol电子,个数为2NA或12.04×1023,故答案为:2NA或12.04×1023.
点评 本题考查氧化还原反应,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意从化合价的角度及电子守恒角度解答该题,难度不大.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
13.一定温度下,在2L密闭容器中加入4.0molA和6.0molB,发生如下可逆反应:2A(g)+3B(g)?4C(g)+D(g).反应10 min后达到平衡,此时D的浓度为0.5molL-1.下列说法正确的是( )
| A. | 前10min反应的平均速率v(C)=0.1 mol/(L•min) | |
| B. | 反应达到平衡时B的平衡浓度是1.5 mol•L-1 | |
| C. | 恒温下,将反应容器体积压缩为原来的一半,则D的平衡浓度小于1.0 mol•L-1 | |
| D. | 10 min后在容器中加入A,重新建立平衡时A的转化率一定大于50% |
8.下列关于氯水的叙述正确的是( )
| A. | 新制氯水中只含Cl2和H2O分子 | |
| B. | 新制氯水不能使干燥的有色布条褪色 | |
| C. | 光照氯水有气泡逸出,该气体是Cl2 | |
| D. | 新制氯水可使蓝色石蕊试纸先变红后褪色 |
13.20世纪90年代,国际上提出了“预防污染”的新概念.“绿色化学”是预防污染的基本手段,下列各项中属于“绿色化学”的是( )
| A. | 对燃烧煤时产生的尾气进行除硫处理 | |
| B. | 往已经酸化的土壤撒石灰中和 | |
| C. | 煤燃烧时鼓入足量空气 | |
| D. | 将煤除硫后再燃烧 |
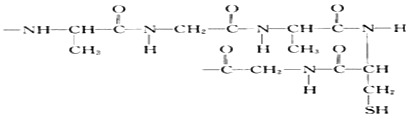
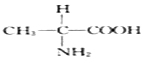
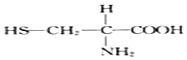
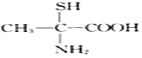
 掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置.
 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: