题目内容
氮化硅(氮显-3价,硅显+4价)是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上曾普遍采用高纯硅与纯氮在1300℃时反应获得.
(1)写出N的原子结构示意图 和氮化硅的化学式 .
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应.试推测该陶瓷被氢氟酸腐蚀的化学方程式 .
(3)现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为 .
(1)写出N的原子结构示意图
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应.试推测该陶瓷被氢氟酸腐蚀的化学方程式
(3)现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为
考点:无机非金属材料
专题:碳族元素
分析:(1)氮原子核内有7个质子,核外有7个电子分布在2个电子层;氮原子与硅原子通过共价键结合成原子晶体氮化硅,氮显-3价,硅显+4价,正负化合价代数和为0写出化学式;
(2)陶瓷被氢氟酸腐蚀生成四氟化硅和氟化铵;
(3)四氯化硅和氮气、氢气反应生成氮化硅和氯化氢.
(2)陶瓷被氢氟酸腐蚀生成四氟化硅和氟化铵;
(3)四氯化硅和氮气、氢气反应生成氮化硅和氯化氢.
解答:
解:(1)N的原子结构示意图为 ,氮化硅中氮显-3价,硅显+4价,依据化合价代数和为0,可知氮化硅中氮原子数4个,硅原子数3个,化学式为:Si3N4;
,氮化硅中氮显-3价,硅显+4价,依据化合价代数和为0,可知氮化硅中氮原子数4个,硅原子数3个,化学式为:Si3N4;
故答案为: ;Si3N4;
;Si3N4;
(2)陶瓷被氢氟酸腐蚀生成四氟化硅和氟化铵,反应的化学方程式为:Si3N4+16HF=3SiF4↑+4NH4F;
故答案为:Si3N4+16HF=3SiF4↑+4NH4F;
(3)四氯化硅和氮气、氢气反应生成氮化硅和氯化氢,化学方程式为3SiCl4+2N2+6H2═Si3N4+12HCl;
故答案为:3SiCl4+2N2+6H2═Si3N4+12HCl.
 ,氮化硅中氮显-3价,硅显+4价,依据化合价代数和为0,可知氮化硅中氮原子数4个,硅原子数3个,化学式为:Si3N4;
,氮化硅中氮显-3价,硅显+4价,依据化合价代数和为0,可知氮化硅中氮原子数4个,硅原子数3个,化学式为:Si3N4;故答案为:
 ;Si3N4;
;Si3N4;(2)陶瓷被氢氟酸腐蚀生成四氟化硅和氟化铵,反应的化学方程式为:Si3N4+16HF=3SiF4↑+4NH4F;
故答案为:Si3N4+16HF=3SiF4↑+4NH4F;
(3)四氯化硅和氮气、氢气反应生成氮化硅和氯化氢,化学方程式为3SiCl4+2N2+6H2═Si3N4+12HCl;
故答案为:3SiCl4+2N2+6H2═Si3N4+12HCl.
点评:本题考查了原子结构示意图的书写、化学式、化学方程式的书写,题目难度不大,根据原子的结构和物质的性质解答,方程式书写时,应注意依据原子个数守恒配平.

练习册系列答案
相关题目
下列关于FeCl3溶液和Fe(OH)3胶体的说法中正确的是( )
| A、都呈红褐色 |
| B、向Fe(OH)3胶体中滴加几滴浓盐酸,可能看到有沉淀产生 |
| C、利用滤纸过滤的方法可以分离两者 |
| D、微粒大小都在1~100nm之间 |
除去苯中的少量苯酚杂质的通常方法是( )
| A、加水振荡,静置分层后用分液漏斗分离 |
| B、加NaOH溶液振荡后,静置分液 |
| C、加溴水振荡后,过滤 |
| D、加CCl4振荡后,静置分液 |
下列各项表达中不正确的是( )
| A、Be2+中的电子数和质子数之比一定为1:2 |
| B、D216O中,质量数之和是质子数之和的两倍 |
| C、在氮原子中,质子数为7而中子数不一定为7 |
D、Cl-的结构示意图为: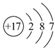 |
