题目内容
15.反应4A(s)+3B(g)=2C(g)+D(g),经2min后,B的浓度减少了0.6mol/L.下列反应速率的表示正确的是( )| A. | 用A表示的反应速率是0.4 mol/(L•min) | |
| B. | 用B表示的反应速率是0.3 mol/(L•min) | |
| C. | 2 min末时的反应速率,用B表示是0.3 mol/(L•min) | |
| D. | 用D表示的反应速率为0.1 mol/L |
分析 A.化学反应速率表示单位时间内浓度的变化量,固体或纯液体的浓度一般视为常数,一般也不用固体或纯液体来表示反应速;
B.根据△c(B)=$\frac{△c(B)}{△t}$计算;
C.化学反应速率为一段时间内平均速率,不是即时速率;
D.反应速率的单位是mol/(L•min).
解答 解:A.物质A是固体,浓度不变,不能用A表示该反应的反应速率,故A错误;
B.△c(B)=$\frac{△c(B)}{△t}$=$\frac{0.6mol/L}{2min}$=0.3mol/(L?min),故B正确;
C.2min末的反应速率为即时速率,用B表示速率0.3mol/(L?min),是2min内的平均速率,故C错误;
D.反应速率的单位是mol/(L•min),故D错误.
故选B.
点评 本题考查对化学反应速率的理解及有关计算,难度不大,化学反应速率为一段时间内平均速率,不是即时速率.

练习册系列答案
相关题目
5.如下性质的递变中,不正确的是( )
| A. | HCl、H2S、PH3的稳定性依次减弱 | |
| B. | HClO4、H2SO4、H3PO4的酸性依次减弱(相同条件下) | |
| C. | CsOH、KOH、LiOH的碱性依次增强 | |
| D. | Na+、Mg2+、Al3+的离子半径逐渐减小 |
6. 如图为直流电源电解稀Na2SO4水溶液的装置.通电后在石墨电极a和b附近分别滴加几滴石蕊溶液.下列实验现象描述正确的( )
如图为直流电源电解稀Na2SO4水溶液的装置.通电后在石墨电极a和b附近分别滴加几滴石蕊溶液.下列实验现象描述正确的( )
 如图为直流电源电解稀Na2SO4水溶液的装置.通电后在石墨电极a和b附近分别滴加几滴石蕊溶液.下列实验现象描述正确的( )
如图为直流电源电解稀Na2SO4水溶液的装置.通电后在石墨电极a和b附近分别滴加几滴石蕊溶液.下列实验现象描述正确的( )| A. | 逸出气体的体积,a电极的小于b电极的 | |
| B. | 一电极逸出无味气体,另一电极逸出刺激性气体 | |
| C. | a电极附近呈红色,b电极附近呈蓝色 | |
| D. | a电极附近呈蓝色,b电极附近呈红色 |
7.反应CH3OH ( l )+NH3( g )═CH3NH2( g )+H2O ( g )在某温度自发向右进行,若反应|△H|=17kJ/mol,|△H-T△S|=17kJ/mol,对于该反应下列关系正确的是( )
| A. | △H>0,△H-T△S<0 | B. | △H<0,△H-T△S>0 | C. | △H>0,△H-T△S>0 | D. | △H<0,△H-T△S<0 |
17.3-氯戊烷是一种有机合成中间体,下列有关3-氯戊烷的叙述正确的是( )
| A. | 3-氯戊烷的分子式为C5H9Cl3 | B. | 3-氯戊烷属于烷烃 | ||
| C. | 3-氯戊烷能发生取代反应 | D. | 3-氯戊烷的同分异构体共有6种 |

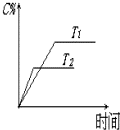 可逆反应aA(s)+bB(g)?c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)如图.下列叙述一定正确的是B
可逆反应aA(s)+bB(g)?c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)如图.下列叙述一定正确的是B