题目内容
7.反应CH3OH ( l )+NH3( g )═CH3NH2( g )+H2O ( g )在某温度自发向右进行,若反应|△H|=17kJ/mol,|△H-T△S|=17kJ/mol,对于该反应下列关系正确的是( )| A. | △H>0,△H-T△S<0 | B. | △H<0,△H-T△S>0 | C. | △H>0,△H-T△S>0 | D. | △H<0,△H-T△S<0 |
分析 反应能自发进行,应满则△G=△H-T•△S<0,以此解答该题.
解答 解:该反应在一定温度下能够自发的向右进行,这说明△H-T△S一定是小于0,根据方程式可知该反应的△S>0,所以如果△H<0,则该反应在任何温度下都是自发进行的,而该反应在一定温度下能够自发的向右进行,因此该反应的反应热△H>0,
故选A.
点评 该题是基础性试题的考查,难度不大.该题的关键是掌握△G=△H-T•△S,并能灵活运用即可,有利于培养学生的逻辑思维能力.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
18.已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
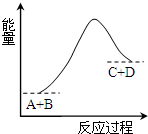

| A. | 该反应反应物A的能量大于生成物D的能量 | |
| B. | 该反应为吸热反应 | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 该反应只有在加热条件下才能进行 |
15.反应4A(s)+3B(g)=2C(g)+D(g),经2min后,B的浓度减少了0.6mol/L.下列反应速率的表示正确的是( )
| A. | 用A表示的反应速率是0.4 mol/(L•min) | |
| B. | 用B表示的反应速率是0.3 mol/(L•min) | |
| C. | 2 min末时的反应速率,用B表示是0.3 mol/(L•min) | |
| D. | 用D表示的反应速率为0.1 mol/L |
12.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.下列说法正确的是( )
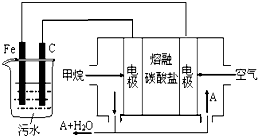

| A. | Fe为阳极,其电极反应为:Fe-3e-+3OH-=Fe(OH)3↓ | |
| B. | 通入甲烷的电极为负极,其电极反应为:CH4-8e-+10OH-=CO32-+7H2O | |
| C. | 为了使该燃料电池长时间稳定运行,电池工作时必须 有部分A物质参加循环.A物质是CO2 | |
| D. | 实验过程中,若在阴极产生了4.48 L气体,则电路中通过的电子个数为0.4NA |
9.下列关于有机物的说法中,错误的是( )
| A. | 乙烯常温下是气体,聚乙烯常温下是固体 | |
| B. | 苯可做有机溶剂 | |
| C. | 乙醇和乙烯都能发生加成反应 | |
| D. | 油脂可用来制造肥皂 |
10.设NA为阿佛加德罗常数的值,下列叙述正确的是( )
| A. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3mol I2转移的电子数为5NA个 | |
| B. | 电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g | |
| C. | 在反应3Cl2+8NH3═6NH4Cl+N2中,有1.2NA个电子发生转移,则被氧化的氨气的质量是27.2 g | |
| D. | 等物质的量的CH4和CO所含分子数均为NA |
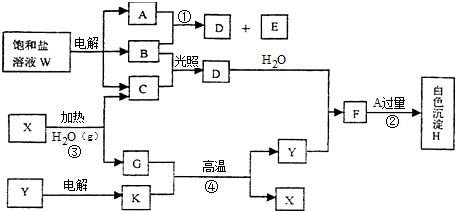
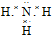 ,B的晶体类型是分子晶体.
,B的晶体类型是分子晶体.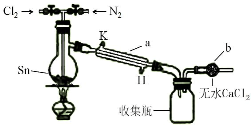 四氯化锡(SnCl4)在电子、化工等领域有重要用途.某兴趣小组拟用Sn和Cl2反应制备SnCl4.
四氯化锡(SnCl4)在电子、化工等领域有重要用途.某兴趣小组拟用Sn和Cl2反应制备SnCl4.