题目内容
8.把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是( )| A. | 盐酸的浓度 | B. | 铝条的表面积 | C. | 溶液的温度 | D. | 加少量NaCl固体 |
分析 过量稀盐酸,Al完全反应,不改变温度、接触面积、盐酸的浓度等,则不影响反应速率,以此来解答.
解答 解:A.改变H+的浓度,反应速率变化,故A不选;
B.改变接触面积,反应速率变化,故B不选;
C.改变温度,反应速率变化,故C不选;
D.加入少量NaCl固体改变Cl-的浓度,对H+的浓度无影响,则Al与盐酸反应生成氢气的速率不变,故D选;
故选D.
点评 本题考查影响反应速率的因素,明确温度、浓度、接触面积对反应速率的影响即可解答,注意反应的实质,题目难度不大.

练习册系列答案
相关题目
19.如图为离子晶体空间构型示意图,则离子晶体的组成表达式不正确的是( )
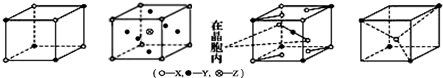

| A. | XY | B. | XY2Z | C. | XY3 | D. | XY2 |
3.下列化学用语表示正确的是( )
| A. | CO2的电子式为: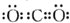 | |
| B. | S2-的离子离子结构示意图是: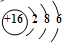 | |
| C. | 原子核内有18个中子的氯原子:3518Cl | |
| D. | HBr电子式为: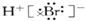 |
13.按碳骨架分类,下列说法正确的是( )
| A. | 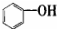 属于醇类化合物 属于醇类化合物 | B. | 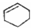 属于芳香族化合物 属于芳香族化合物 | ||
| C. | CH 3CH(CH 3 )2 属于链状化合物 | D. | 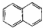 属于脂环化合物 属于脂环化合物 |
20.SO2溶于水所得溶液的性质为( )
| A. | 有氧化性,无还原性,无酸性 | B. | 无氧化性,有还原性,无酸性 | ||
| C. | 有氧化性,有还原性,有酸性 | D. | 无氧化性,有还原性,有酸性 |
18.根据有关概念,推断下列说法中正确的是( )
| A. | NaCl发生状态变化时,一定会破坏离子键 | |
| B. | 元素的非金属性越强,单质的活泼性一定越强 | |
| C. | 物质中分子间的作用力越大,分子越稳定 | |
| D. | 只含有共价键的物质一定是共价化合物 |
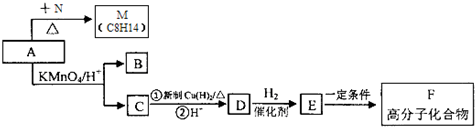
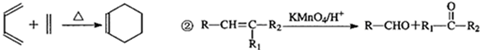
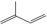 ,A与Br2按物质的量比l:l 发生加成反应,请写出生成的所有产物的结构简式为CH2BrCBr(CH3)CH=CH2、CH2=C(CH3)CHBrCH2Br、CH2BrC(CH3)=CHCH2Br(不考虑顺反异构).
,A与Br2按物质的量比l:l 发生加成反应,请写出生成的所有产物的结构简式为CH2BrCBr(CH3)CH=CH2、CH2=C(CH3)CHBrCH2Br、CH2BrC(CH3)=CHCH2Br(不考虑顺反异构). .
.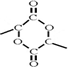 含有三元环:
含有三元环: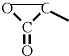 .
.