题目内容
【题目】以有机化合物A为初始原料,合成有机化合物C和F的路线如图所示:
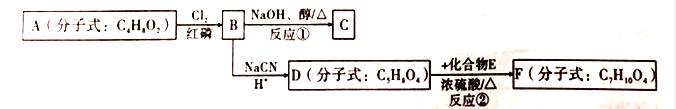
已知以下信息:
①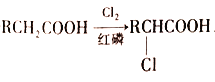 ,R-Cl
,R-Cl![]() R—COOH,其中R表示烃基;
R—COOH,其中R表示烃基;
②D的核磁共振氢谱有两种不同化学环境的氢;
③F为七元环状化合物。
回答下列问题:
(1)A中含有的官能团名称为________;1molA完全燃烧消耗O2________mol.
(2)判断反应类型:反应①为_________;反应②为_________。
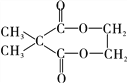
(3)E的结构简式为_________;F的结构简式为_________。
(4)由B生成C的化学方程式为_________。
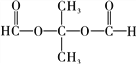
(5)请写出满足下列条件的D的2种链状同分异构体的结构简式: _________。
①可发生水解反应;②核磁共振氢谱显示有两组峰,且峰面积之比为1:3。
(6)利用该合成路线中的有关信息,写出以乙醇为初始原料,其他无机试剂任选,制备有机化合物CH2=CHCOOH的合成路线流程图:(流程图示例:CH3CH2OH![]() H2C=CH2
H2C=CH2![]() BrH2C—CH2Br)________________
BrH2C—CH2Br)________________
【答案】 羧基 5 消去反应 酯化反应(或取代反应) ![]()
![]()
 、
、![]()
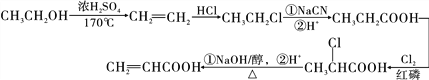
【解析】结合已知条件,D的核磁共振氢谱有两种不同化学环境的氢,D结构高度对称且含有羧基,羧基中有一种氢,则D的结构简式为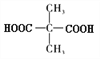 ,则B为
,则B为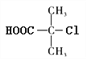 ,A为
,A为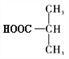 ;
; 在氢氧化钠的醇溶液中加热发生消去反应生成C为
在氢氧化钠的醇溶液中加热发生消去反应生成C为![]() ;
; 与化合物E在浓硫酸催化下发生酯化反应生成七元环状化合物F,根据F的分子式可推知F为
与化合物E在浓硫酸催化下发生酯化反应生成七元环状化合物F,根据F的分子式可推知F为 ;则E为
;则E为![]() 。(1)A为
。(1)A为 ,含有的官能团名称为羧基;A的分子式为C4H8O2,根据有机物CxHyOz耗氧x+
,含有的官能团名称为羧基;A的分子式为C4H8O2,根据有机物CxHyOz耗氧x+![]() -
-![]() 计算可知,1molA完全燃烧消耗O2(4+
计算可知,1molA完全燃烧消耗O2(4+![]() )mol=5mol;(2)反应①为
)mol=5mol;(2)反应①为 在氢氧化钠的醇溶液中加热发生消去反应生成
在氢氧化钠的醇溶液中加热发生消去反应生成![]() ;反应②为
;反应②为 与
与![]() 在浓硫酸催化下发生酯化反应,也属于取代反应;(3)E的结构简式为
在浓硫酸催化下发生酯化反应,也属于取代反应;(3)E的结构简式为![]() ;F的结构简式为
;F的结构简式为 ;(4)由
;(4)由![]() ;(5)满足下列条件的D的链状同分异构体:①可发生水解反应,则应该为酯;②核磁共振氢谱显示有两组峰,且峰面积之比为1:3,则高度对称,则应该为两个甲基,则结构简式为
;(5)满足下列条件的D的链状同分异构体:①可发生水解反应,则应该为酯;②核磁共振氢谱显示有两组峰,且峰面积之比为1:3,则高度对称,则应该为两个甲基,则结构简式为 、
、![]() ;(6)根据流程图示例:CH3CH2OH
;(6)根据流程图示例:CH3CH2OH![]() H2C=CH2
H2C=CH2![]() BrH2C—CH2Br,结合题干信息RCH2COOH
BrH2C—CH2Br,结合题干信息RCH2COOH![]()
![]() ,R—Cl
,R—Cl![]() R—COOH,以及合成路线中的相关信息完成以乙醇为初始原料,制备CH2=CHCOOH的合成路线流程图如下:
R—COOH,以及合成路线中的相关信息完成以乙醇为初始原料,制备CH2=CHCOOH的合成路线流程图如下: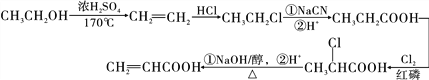 。
。

【题目】NO2、NO、CO、NO2-等是常见大气污染物和水污染物,研究NO2、NO、CO、NO2-等的处理对建设美丽中国具有重要意义。
已知:①NO2+CO![]() CO2+NO,该反应的平衡常数为K1(下同)。断开1mol下列物质的所有化学键时所消耗能量分别为:
CO2+NO,该反应的平衡常数为K1(下同)。断开1mol下列物质的所有化学键时所消耗能量分别为:
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②![]() N2(g)+
N2(g)+ ![]() O2(g)
O2(g)![]() NO(g) △H=+89.75kJ/mol,K2
NO(g) △H=+89.75kJ/mol,K2
③2NO(g)+O2(g)![]() 2NO2(g) △H=-112.3kJ/mol,K3
2NO2(g) △H=-112.3kJ/mol,K3
写出NO与CO反应生成无污染气体的热化学方程式:_____________,此热化学方程式的平衡常数K=_______(用K1、K2、K3表示)
(2)污染性气体NO2与CO在一定条件下的反应为2NO2+4CO![]() 4CO2+N2,某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1个大气压,5秒时反应达到平衡,容器的压强变为原来的
4CO2+N2,某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1个大气压,5秒时反应达到平衡,容器的压强变为原来的![]() ,则反应开始到平衡时CO的平均反应速率v(CO)=_______。若此温度下,某时刻则得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围为________。
,则反应开始到平衡时CO的平均反应速率v(CO)=_______。若此温度下,某时刻则得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围为________。
(3)研究发现:NOx是雾霾的主要成分之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。已知:4NH3(g)+6NO(g)=5N2(g)+6H2O(g) △H=-1810kJ/mol
①相同条件下,在2L恒容密闭容器中,选用不同的催化剂,上述反应产生N2的物质的量随时间变化的情况如图所示。
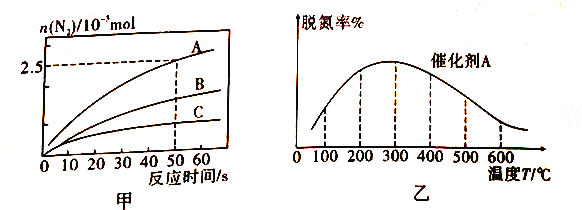
a.在催化剂A作用下,反应达到平衡的标志是_____(填序号)。
A.4v(NH3)正=6v(H2O)逆
B.容器内总压强不再改变
C.容器内密度不再改变
D.NO 和H2O(g)浓度相等
E.容器内平均摩尔质量不再改变
b.在A、B,C 三种催化剂下,清除氮氧化物反应的活化能分别表示为Ea(A)、Ea(B)、Ea(C),根据图甲所示曲线,判断三种催化剂条件下,活化能由大到小的顺序为________。
②在氨气足量时,反应在催化剂A 作用下,经过相同时间,测得脱氮潮殖反应温度的变化情况如图乙所示,据图可知,自相同的时间内,温度对脱氮率的影响及可他的原因是________。(已知A、B催化剂在此温度范围内不失效)。
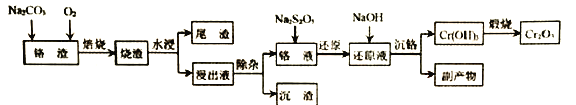
【题目】氨基磺酸镍[Ni(H2NSO3)2]是工业电镀镍所必需的化工原料,某科研小组先用尿素、SO3合成中间体氨基磺酸(H2NSO3H),再用氨基磺酸、金属镍和双氧水反应来合成氨基磺酸镍。已知磺化制氨基磺酸反应原理和整个过程的流程图如下:
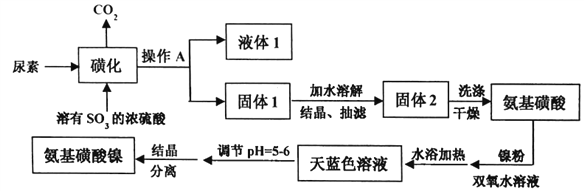
①CO(NH2)2(s)+SO3(g)→H2NCONHSO3H(s) △H<0
②H2NCONHSO3H (s)+ H2SO4→2H2NSO3H (s)+ CO2↑
已知物质的部分性质如下:
物质 | 溶解性 | 稳定性 | 酸碱性 |
氨基磺酸 | 溶于水、不溶于乙醇 | pH较低时发生水解生成NH4HSO4 | 强酸性 |
氨基磺酸镍 | 溶于水、乙醇 | 高于110℃时分解 | 酸性 |
请回答
(1)操作A的名称是_________液体1的主要成分是_______(填化学式)。
(2)“磺化”过程的温度与产率的关系如下图。温度高于80℃时氨基磺酸的产率会降低,原因一是升高温度平衡逆向移动,原因二是__________。
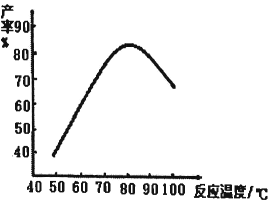
(3)写出制备氨基磺酸镍的化学方程式____________________。
(4)写出固体2洗涤的操作过程___________________。
(5)流程图中“天蓝色溶液”需要调节pH=5~6的原因是___________。