题目内容
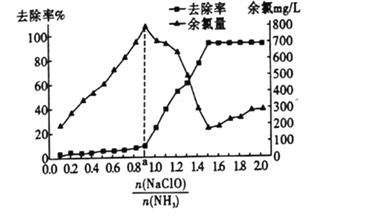
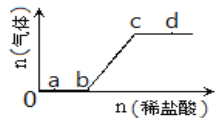
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是(已知硝酸可将Fe2+氧化)( )
A. a点对应的溶液中:Na+、OH-、SO42-、NO3- B. b点对应的溶液中:K+、Ag+、MnO4-、NO3-
C. c点对应的溶液中:Fe2+、Ca2+、NO3-、Cl- D. d点对应的溶液中:K+、Fe2+、NO3-、SO42-
【答案】C
【解析】
a点溶液中含有CO32-和HCO3-,b点全部为HCO3-,c点恰好完全反应生成NaCl,溶液呈中性,d点盐酸过量,呈酸性,A.a点溶液中含有CO32-和HCO3-,HCO3-与OH-反应不能大量共存,选项A错误;B.b点全部为HCO3-,Al3+与HCO3-发生互促水解反应而不能大量共存,选项B错误;C.c点恰好完全反应生成NaCl,溶液呈中性,离子之间不发生反应,在溶液中能够大量共存,选项C正确;D.d点呈酸性,酸性条件下,NO3-与Fe2+发生氧化还原反应而不能大量共存,选项D错误;答案选C。

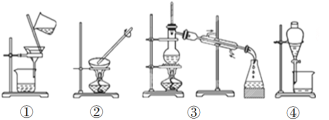
【题目】Ⅰ、实验室要配制物质的量浓度为0.1 mol/L的NaOH溶液480 mL
(1)填表:
配制时应称量NaOH的质量/g | 已给仪器 | 配制时除已给仪器外还需要的其他仪器 |
__________ | 烧杯、药匙、托盘天平 | ____________________________ |
(2)若要计算该溶液溶质的质量分数,还需要的一个条件是______________(用文字说明)。
(3)下列操作对配制的NaOH溶液浓度有偏高影响的是_________________(填字母)
A.称量NaOH固体时,露置在空气的时间过长
B.选用的容量瓶内有少量的蒸馏水
C.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
D.在定容时仰视容量瓶刻度线
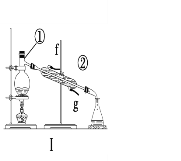
Ⅱ、实验室用下图几个实验装置,可快速制取少量气体,并进行相关性质实验。

(1)若 A为30%H2O2溶液,B为MnO2 ,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程式:______________________________________。
(2)若A中装有浓盐酸,B中装有固体KMnO4 ,C中盛有KI淀粉溶液,旋开E后,B中出现黄绿色气体。已知1 mol KMnO4发生反应时转移5mol电子。则B中发生反应的离子方程式是:_______;C中的现象是:___________。