题目内容
7.下列化学用语正确的是( )| A. | NaCl的电子式: | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | Mg原子结构示意图: | |
| D. | 硫酸铁的电离方程式 Fe2(SO4)3=2Fe3++3SO42ˉ |
分析 A.NaCl是离子化合物,由Na+、Cl-组成,电子式中需要标出阴阳离子所带电荷;
B.结构简式需标出官能团;
C.原子结构示意图中核外电子数与核电荷数相等;
D.硫酸铁为强电解质,在溶液中完全电离出铁离子和硫酸根离子.
解答 解:A.氯化钠为离子化合物,氯离子带电荷并需用方括号括起来,钠离子用离子符号表示,氯化钠的电子式为 ,故A错误;
,故A错误;
B.乙烯的官能团是C=C双键,其正确的结构简式为:CH2=CH2,故B错误;
C.镁原子的核电荷数与核外电子总数相等,最外层电子数为2,镁原子正确的结构示意图为: ,故C错误;
,故C错误;
D.硫酸铁在溶液中完全电离,其电离方程式为:Fe2(SO4)3=2Fe3++3SO42-,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及电子式、结构简式、原子结构示意图等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
2.卤素单质的性质活泼,卤素的化合物应用广泛,运用化学反应原理研究卤族元素的有关性质具有重要意义.
(1)下列关于氯水的叙述正确的是AEF(填写序号).
A.氯水中存在两种电离平衡
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25℃时有关弱酸的电离平衡常数:
写出84消毒液(主要成分为NaClO)露置在空气中发生反应的有关化学方程式NaClO+CO2+H2O═HClO+NaHCO3.若将84消毒液与洁厕剂(含有浓盐酸)混合使用可能会导致中毒,请用离子方程式解释有关原因ClO-+Cl-+2H+═Cl2↑+H2O.
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.工业上制备ClO2的反应原理常采用:2NaClO3+4HCl(浓)═2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是B(填序号).
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ClO2,则转移电子的物质的量为0.1mol.
③ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.现用ClO2将CN-氧化,有两种气体生成,其离子反应方程式为2ClO2+2CN-=N2↑+2CO2↑+2Cl-.
(1)下列关于氯水的叙述正确的是AEF(填写序号).
A.氯水中存在两种电离平衡
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=3.0×10-8 | K1=4.4×10-7,K2=4.7×10-11 |
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.工业上制备ClO2的反应原理常采用:2NaClO3+4HCl(浓)═2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是B(填序号).
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ClO2,则转移电子的物质的量为0.1mol.
③ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.现用ClO2将CN-氧化,有两种气体生成,其离子反应方程式为2ClO2+2CN-=N2↑+2CO2↑+2Cl-.
19.洗涤下列试管时,选用的试剂(括号中物质)不妥当的是( )
| A. | 做过KMn04分解反应实验的试管(浓盐酸) | |
| B. | 做过木炭还原氧化铜实验的试管(硝酸) | |
| C. | 做过银镜反应实验的试管(氨水) | |
| D. | 做过Na2S2O3与稀硫酸反应的试管(二硫化碳) |
2.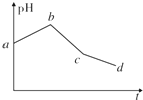 将物质的量浓度相等的KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如上图所示,则下列说法正确的是( )
将物质的量浓度相等的KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如上图所示,则下列说法正确的是( )
 将物质的量浓度相等的KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如上图所示,则下列说法正确的是( )
将物质的量浓度相等的KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如上图所示,则下列说法正确的是( )| A. | ab段表示电解过程中H+被还原,pH上升 | |
| B. | 电解开始时阳极先发生电极反应2Cl--2e-═Cl2↑ | |
| C. | 电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液恢复至原来的浓度 | |
| D. | 原混合溶液中KCl和CuSO4的浓度之比恰好为2:1 |
19.下列有关说法正确的是( )
| A. | 在任何条件下,纯水都呈中性 | |
| B. | 电离平衡常数Ka越小,表示弱电解质电离能力越强 | |
| C. | 为保存FeCl3溶液,要在溶液中加少量硫酸 | |
| D. | 明矾溶液蒸干得到的固体为Al(OH)3 |
16.pH=12的NaOH溶液和pH=10的NaOH溶液等体积混合后溶液的( )
| A. | pH=11 | B. | pH=10.3 | ||
| C. | c(H+)=2×10-12 mol•L-1 | D. | c(H+)=(10-12+10-10)/2 mol•L-1 |
17.如图所示的甲、乙两个装置中(常温),胶头滴管中吸入某种液体,圆底烧瓶中充入(或放入)另一种物质,挤压胶头滴管中液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则下列选项中所用试剂合理的是( )

| 选项 | 甲 | 乙 | ||
| 滴管中 | 烧瓶中 | 滴管中 | 烧瓶中 | |
| A | 水 | 钠 | 饱和碳酸钠溶液 | CO2 |
| B | 水 | 过氧化钠 | 饱和碳酸氢钠溶液 | CO2 |
| C | NaOH溶液 | 碳酸氢钠 | 澄清石灰水 | 碳酸氢钠 |
| D | 稀盐酸 | 碳酸氢钠 | FeCl3溶液 | Cu |

| A. | A | B. | B | C. | C | D. | D |