题目内容
下列实验操作与所得实验结论一致的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某溶液中加入盐酸,产生CO2气体 | 说明原溶液中一定为Na2CO3 |
| B | 向某溶液中滴入氢氧化钠溶液,产生蓝色沉淀 | 说明原溶液中一定含有Cu2+ |
| C | 向某溶液中滴入氯化钡溶液,产生白色沉淀 | 说明原溶液中一定含有Ag+ |
| D | 向某溶液中先滴入盐酸,再滴入氯化钡溶液,产生白色沉淀 | 说明原溶液中一定含有SO42- |
| A、A | B、B | C、C | D、D |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:A.NaHCO3溶液加入盐酸,也可产生CO2气体;
B.氢氧化铜为蓝色沉淀;
C.可能生成硫酸钡、碳酸钡等沉淀;
D.先加盐酸,可排除阴离子以及碳酸根等离子的影响.
B.氢氧化铜为蓝色沉淀;
C.可能生成硫酸钡、碳酸钡等沉淀;
D.先加盐酸,可排除阴离子以及碳酸根等离子的影响.
解答:
解:A.HCO3-也能与稀盐酸反应生成二氧化碳气体,故A错误;
B.氢氧化铜为蓝色沉淀,可证明原溶液中一定含有Cu2+,故B正确;
C.可能生成硫酸钡、碳酸钡等沉淀,应加入硝酸酸化的硝酸银,故C错误;
D.先加盐酸,可排除阴离子以及碳酸根等离子的影响,如加入氯化钡生成沉淀,可说明原溶液中一定含有SO42-,故D正确.
故选BD.
B.氢氧化铜为蓝色沉淀,可证明原溶液中一定含有Cu2+,故B正确;
C.可能生成硫酸钡、碳酸钡等沉淀,应加入硝酸酸化的硝酸银,故C错误;
D.先加盐酸,可排除阴离子以及碳酸根等离子的影响,如加入氯化钡生成沉淀,可说明原溶液中一定含有SO42-,故D正确.
故选BD.
点评:本题考查化学实验的评价,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,题目难度中等,注意离子的检验要首先排除其它离子的干扰.

练习册系列答案
相关题目
向一定量Fe、Fe2O3的混合物中加入250mL 2mol?L-1的HNO3溶液,反应完成后生成1.12L(标准状况下)NO气体,再向反应后溶液中加入1mol?L-1 NaOH溶液,要使铁元素完全沉淀下来,所加入NaOH溶液体积最少是( )
| A、450 mL |
| B、500 mL |
| C、400 mL |
| D、不能确定 |
对于可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,下列研究结果和示意图相符的是( )
| A | B | C | D | |
| 研究 结果 | 压强对反应的影响 | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 | 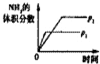 | 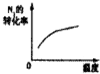 | 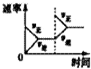 |  |
| A、A | B、B | C、C | D、D |
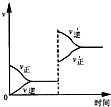 若平衡体系A+B═C+D,增大压强时反应速率变化如图所示.则下列关于各物质状态的说法正确的是( )
若平衡体系A+B═C+D,增大压强时反应速率变化如图所示.则下列关于各物质状态的说法正确的是( )| A、A、B、C、D都是气体 |
| B、C、D都是气体,A、B中有一种是气体 |
| C、A、B都不是气体,C、D中有一种是气体 |
| D、A、B都是气体,C、D中有一种是气体 |
某学生设计了如图所示的方法对A盐溶液进行鉴定由此分析,下列结论中不正确的是( )
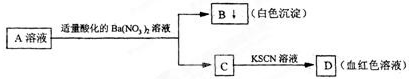

| A、A中一定有Fe3+ |
| B、C中一定有Fe3+ |
| C、A可能为Fe2(SO4)3 |
| D、B一定为BaSO4 |
某有机物完全燃烧,生成的产物只有CO2和H2O.将6g该有机物完全燃烧的产物通过浓硫酸,浓硫酸增重7.2g,再通过氢氧化钠溶液,又增重13.2g.该有机物的分子式为( )
| A、C4H10 |
| B、C3H8 |
| C、C3H8O |
| D、C2H4O2 |
据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应的化学方程式为:2CO2(g)+6H2(g)═CH3CH2OH(g)+3H2O(g).下列叙述正确的是( )
| A、当v(CO2)=2v(CH3CH2OH)时,反应一定达到平衡状态 |
| B、增大压强,可提高CO2和H2的转化率 |
| C、当平衡向正反应方向移动时,平衡常数一定增大 |
| D、移去生成的乙醇和水,可以加快反应速率 |