题目内容
【题目】结合元素周期表,回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图 1 中用实线补全元素周期表 的边界____________
(2)表中所列元素,属于短周期元素的有____________;属于主族元素的有____________;g 元素位于第____________ 周期____________ 族;i 元素位于第____________ 周期____________族.
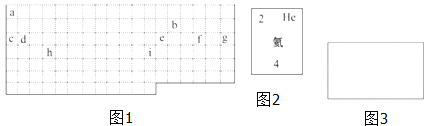
(3)元素 f 是第_______周期、第_______ 族元素,请在如图 3 所示的方框中按 氦元素(图 2)的式样写出该元素的原子序数、元素符号、元素名称、相对原子 质量_______.
【答案】 H、C、Na、Mg、Al、S、ArH、C、Na、Mg、Al、S三零四IIB三ⅥA
H、C、Na、Mg、Al、S、ArH、C、Na、Mg、Al、S三零四IIB三ⅥA
【解析】
(1)上边界为短周期元素,一周期有2种元素,二、三周期有8种元素,以此分析;(2)长周期为四、五、六、七周期;g为Ar元素,原子序数为18;i为Zn元素,原子序数为30;(3)f为S元素,位于第三周期第ⅥA族,质子数为16,相对原子质量为32。
(1)上边界为短周期元素,一周期有2种元素,二、三周期有8种元素,表示元素周期表的部分边界如图:
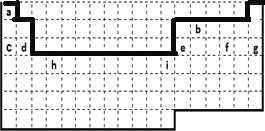 , 故答案为:
, 故答案为: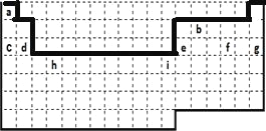 。
。
(2)长周期为四、五、六、七周期,由图可知,a为H、b为C、c为Na、d为Mg、e为Al、f为S、g为Ar,均为短周期元素,H、C、Na、Mg、Al、S为主族元素,g为Ar元素,原子序数为18,位于周期表第三周期零族;i为Zn元素,原子序数为30,位于周期表第四周期IIB族,故答案为:H、C、Na、Mg、Al、S、Ar;H、C、Na、Mg、Al、S;三;零;四;IIB。(3)f为S元素,位于周期表第三周期第ⅥA族,质子数等于原子序数为16,相对原子质量为32,名称为硫,可在方格中表示为 ,故答案为:三;ⅥA;
,故答案为:三;ⅥA; 。
。

 期末集结号系列答案
期末集结号系列答案【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中投入H2和I2,发生反应:H2(g)+I2(g) ![]() 2HI(g)。反应体系中各物质浓度的有关数据如下。
2HI(g)。反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)/(mol·L-1) | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | c |
下列判断不正确的是
A. HI的平衡浓度:a=b>0.004,c=0.008 B. 平衡时,H2的转化率:丁>甲
C. 平衡时,乙中H2的转化率大于20% D. 丙中条件下,该反应的平衡常数K=0.25