题目内容
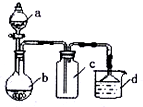 实验室某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中物质 | b中物质 | c中收集气体 | d中物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硝酸 | Cu | NO2 | H2O |
| C | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| D | 浓盐酸 | KClO3 | Cl2 | 澄清石灰水 |
| A、A | B、B | C、C | D、D |
考点:常见气体制备原理及装置选择,气体的收集,尾气处理装置
专题:
分析:根据装置图可知所制备的气体应为固体和液体制备,并用向上排空气法收集以及采用防倒吸的方法进行尾气处理,根据各选项中反应物的状态判断发生装置、气体的性质以及气体要采用防倒吸解答本题.
解答:
解:A.氨气的密度比空气小,不能使用向上排空气法,故A错误;
B.铜与稀硝酸反应需要加热,且产生的气体为NO,不能用水吸收,故B错误;
C.SO2气体的密度比空气大,能使用向上排空气法,SO2气体能与氢氧化钠迅速反应,所以吸收时要防倒吸,故C正确;
D.制取氯气需要加热,氯气的密度比空气大,能使用向上排空气法,氯气用澄清石灰水溶液吸收时不需要防倒吸,故D错误;
故选C.
B.铜与稀硝酸反应需要加热,且产生的气体为NO,不能用水吸收,故B错误;
C.SO2气体的密度比空气大,能使用向上排空气法,SO2气体能与氢氧化钠迅速反应,所以吸收时要防倒吸,故C正确;
D.制取氯气需要加热,氯气的密度比空气大,能使用向上排空气法,氯气用澄清石灰水溶液吸收时不需要防倒吸,故D错误;
故选C.
点评:本题考查化学实验基本原理(气体的制备),实验装置、仪器的使用,难度不大,掌握物质的性质即可解答.

练习册系列答案
相关题目
下列物质中既能跟氢氧化钠反应又能跟盐酸反应的是( )
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3 ⑤NaHSO3.
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3 ⑤NaHSO3.
| A、③④ | B、②③④⑤ |
| C、①③④ | D、全部 |
下列有关溶液组成的描述合理的是( )
| A、弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
| B、酸性溶液中可能大量存在Na+、ClO-、SO42-、I- |
| C、常温下在c(H+)=1×10-13 mol?L-1的溶液中能大量存在Mg2+、Cu2+、SO42-、NO3- |
| D、加入铝粉能产生氢气的溶液中大量存在NH4+、Fe2+、SO42-、NO3- |
下列说法正确的是( )
| A、用光亮洁净的铁丝蘸取某无色溶液,在无色灯焰上灼烧时观察到黄色火焰,则该溶液中一定含Na+,一定不含K+ |
| B、酸、碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应的离子反应都可用H++OH-=H2O来表示 |
| C、实验室常将硫磺撒在汞的表面,以除去不慎洒落的汞 |
| D、Na2O与Na2O2都能和水反应生成NaOH,所以它们都是碱性氧化物 |
在体积固定的绝热密闭容器中,可逆反应NO2(g)+SO2(g)?NO(g)+SO3(g)△H<0达到平衡状态的标志是( )
| A、NO2、SO2、NO和SO3四种气体的物质的量浓度之比为1:1:1:1 |
| B、生成n molSO2同时有n mol SO3消耗 |
| C、K值不再发生变化 |
| D、密闭容器中气体的密度不再发生变化 |