题目内容
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6g固体;向上述滤液中加足量BaCl2溶液,得到 4.66g不溶于盐酸的沉淀.
回答下列问题:
(1)该溶液中一定存在的离子有: ,一定不存在的离子有 .
(2)该溶液中一定存在的阴离子的浓度为 , .
(3)若用质量分数为36.5%,密度为1.2g/ml的浓盐酸配制80mL6mol/L的稀盐酸.回答下列问题
①所需浓盐酸的体积为 mL,配制时需要用到的玻璃仪器有 .
②分析实验中以下操作对所配溶液的浓度有何影响:(填“偏大”、“偏小“或“不受影响”)
A、量取浓盐酸后用蒸馏水洗涤量筒2到3次,将洗涤液转移到容量瓶中, .
B、定容时俯视刻度线, .
C、稀释浓盐酸时烧杯中有少量水, .
回答下列问题:
(1)该溶液中一定存在的离子有:
(2)该溶液中一定存在的阴离子的浓度为
(3)若用质量分数为36.5%,密度为1.2g/ml的浓盐酸配制80mL6mol/L的稀盐酸.回答下列问题
①所需浓盐酸的体积为
②分析实验中以下操作对所配溶液的浓度有何影响:(填“偏大”、“偏小“或“不受影响”)
A、量取浓盐酸后用蒸馏水洗涤量筒2到3次,将洗涤液转移到容量瓶中,
B、定容时俯视刻度线,
C、稀释浓盐酸时烧杯中有少量水,
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:(1)(2)加入过量NaOH溶液,加热,得到0.02mol气体,可知一定存在铵根离子;
红褐色沉淀是氢氧化铁,1.6g固体为三氧化二铁,可知一定有Fe3+,一定没有CO32-;
4.66g不溶于盐酸的沉淀,为硫酸钡沉淀,物质的量为:0.02mol;
根据以上数据推算存在离子,根据电荷守恒推算氯离子的存在及数据.
(3)①根据c=
计算出浓盐酸的物质的量浓度,再根据溶液稀释过程中溶质的物质的量不变计算出配制6moL?L-1的稀盐酸80mL需要浓盐酸的体积;根据实验操作的步骤(计算→量取→稀释、冷却→移液→洗涤→定容→摇匀→装瓶贴签)以及每步操作需要仪器确定需要的仪器;
②根据实验操作对物质的量浓度c=
的影响判断误差.
红褐色沉淀是氢氧化铁,1.6g固体为三氧化二铁,可知一定有Fe3+,一定没有CO32-;
4.66g不溶于盐酸的沉淀,为硫酸钡沉淀,物质的量为:0.02mol;
根据以上数据推算存在离子,根据电荷守恒推算氯离子的存在及数据.
(3)①根据c=
| 1000ρw |
| M |
②根据实验操作对物质的量浓度c=
| n |
| V |
解答:
解:(1)加入NaOH溶液共热有气体和红褐色沉淀,气体为氨气,红褐色沉淀为氢氧化铁,则溶液中一定含有NH4+、Fe3+,根据离子共存可知不含CO32-,加BaCl2溶液生成不溶于盐酸的沉淀,知溶液中含SO42-,
n(NH3)=0.02mol,知n(NH4+)=0.02mol,
n(Fe2O3)=
=0.01mol,知n(Fe3+)=0.02mol,
n(BaSO4)=
=0.02mol,知n(SO42-)=0.02mol,
溶液中NH4+、Fe3+所带正电荷为0.02mol+3×0.02mol=0.08mol,SO42-所带负电荷为2×0.02mol=0.04mol,
据电荷守恒,知溶液中必然大量存在另一种阴离子Cl-,故原溶液中一定含Fe3+、NH4+、SO42-和Cl-,一定不存在CO32-,Al3+和K+不能确定是否存在;
故答案为:Fe3+、NH4+、SO42-和Cl-;CO32-;
(2)硫酸根离子浓度为:
=0.2mol/L,若无Al3+和K+,根据电荷守恒得:NH4+、Fe3+所带正电荷为0.02mol+3×0.02mol=0.08mol,SO42-所带负电荷为2×0.02mol=0.04mol,故氯离子所带负电荷为0.04mol,浓度为:
=0.4mol/L,若存在Al3+和K+,则氯离子浓度大于0.4mol/L;
故答案为:c(SO42-)=0.2mol/L; c(Cl-)≥0.4mol/L;
(3)①质量分数为36.5%,密度为1.20g?cm-3的浓盐酸的物质的量浓度为:
=12mo/L,配制80mL 6moL?L-1的稀盐酸,没有80mL容量瓶,故需选100mL容量瓶,需要浓盐酸的体积为:
=0.05L=50mL.配制顺序是:计算→量取→稀释、冷却→移液→洗涤→定容→摇匀→装瓶贴签,用50mL量筒量取浓盐酸,在烧杯中稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,
所以需要玻璃仪器为:量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,
故答案为:50;量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管;
②A.在操作B中若用水洗涤量筒2-3次,并将洗涤液一并倒入烧杯中:量筒不能洗涤,否则会导致配制的溶液中溶质的物质的量偏大,溶液浓度偏大;
B.定容时俯视,导致加入的蒸馏水体积偏小,配制的溶液体积偏小,溶液浓度偏大;
C.稀释时还需加水,故无影响;
故答案为:偏大;偏大;不受影响.
n(NH3)=0.02mol,知n(NH4+)=0.02mol,
n(Fe2O3)=
| 1.6g |
| 160g/mol |
n(BaSO4)=
| 4.66g |
| 233g/mol |
溶液中NH4+、Fe3+所带正电荷为0.02mol+3×0.02mol=0.08mol,SO42-所带负电荷为2×0.02mol=0.04mol,
据电荷守恒,知溶液中必然大量存在另一种阴离子Cl-,故原溶液中一定含Fe3+、NH4+、SO42-和Cl-,一定不存在CO32-,Al3+和K+不能确定是否存在;
故答案为:Fe3+、NH4+、SO42-和Cl-;CO32-;
(2)硫酸根离子浓度为:
| 0.02mol |
| 0.1L |
| 0.04mol |
| 0.1L |
故答案为:c(SO42-)=0.2mol/L; c(Cl-)≥0.4mol/L;
(3)①质量分数为36.5%,密度为1.20g?cm-3的浓盐酸的物质的量浓度为:
| 1000×1.20×36.5% |
| 36.5 |
| 6mol/L×0.1L |
| 12mol/L |
所以需要玻璃仪器为:量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,
故答案为:50;量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管;
②A.在操作B中若用水洗涤量筒2-3次,并将洗涤液一并倒入烧杯中:量筒不能洗涤,否则会导致配制的溶液中溶质的物质的量偏大,溶液浓度偏大;
B.定容时俯视,导致加入的蒸馏水体积偏小,配制的溶液体积偏小,溶液浓度偏大;
C.稀释时还需加水,故无影响;
故答案为:偏大;偏大;不受影响.
点评:本题考查离子共存和配制一定物质的量浓度的溶液的方法,为高考常见题型和高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意常见离子的性质和反应类型的判断,答题时认真阅读、分析题中数据,合理分析,特别是氯离子的推断,难度中等.注意明确误差分析的方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有两种金属的合金13g,与足量稀硫酸反应后,在标准状况下产生气体11.2L,则组成该合金的金属可能是( )
| A、Mg和Al |
| B、Mg和Zn |
| C、Fe和Zn |
| D、Cu和Fe |
2011年12月江西铜业排污祸及下游,据测定废水中重金属污染物和有毒非金属污染物达二十余种,当地民众重金属中毒病症和奇异怪病时有发生. 废水中的重金属指的是( )
| A、金属单质 | B、金属元素 |
| C、金属铜 | D、金属氧化物 |
在无色透明溶液中,能大量共存的离子组是( )
| A、Cu2+、Na+、SO42-、Cl- |
| B、K+、H+、HCO3-、NO3- |
| C、OH-、HCO3-、Ca2+、Na+ |
| D、Ba2+、Na+、OH-、NO3- |
下列关于溶液中离子浓度的说法正确的是( )
| A、0.1mol.L-1的NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | ||||
B、室温下,将物质的量浓度相等的一元酸HA和KOH等体积混合,溶液的pH=9,则:c(OH-)=c(K+)-c(A-)=
| ||||
C、将HCN和HF溶液混合,达平衡时:c(H+)=
| ||||
| D、等物质的量的CH3COOH和CH3COONa配置成混合溶液,已知其中c(CH3COO-)>c(Na+),则c(CH3COOH)<c(CH3COO-) |
下列离子方程式正确的是( )
| A、铜氨溶液的制备:Cu2-+2NH3.H2O=Cu(NH3)22++2H2O |
| B、氢氧化钡溶液中滴加明矾溶液至Ba2+恰好完全沉淀:Ba2++30H-+SO42-+Al3+=BaSO4↓+Al(OH)3↓ |
C、水杨酸钠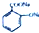 通入过量的CO2; 通入过量的CO2; 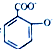 +CO2+H2O→ +CO2+H2O→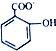 +HCO3- +HCO3- |
| D、在氯化亚铁溶液中加入足量酸性高锰酸钾溶液:5Fe2++8H++Mn04-=5Fe3++Mn2++4H2O |
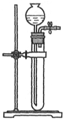 检查装置气密性是化学实验中的重要操作之一.按要求回答下列问题:
检查装置气密性是化学实验中的重要操作之一.按要求回答下列问题: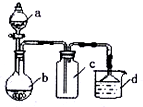 实验室某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质完成相关实验,最合理的选项是( )