题目内容
2.某化学兴趣小组对二氧化碳与氢氧化钠反应后溶液中的溶质进行如下探究:向300mL 1mol/L的NaOH溶液中通入一定量CO2,充分反应后将溶液蒸发结晶,得到一定量的白色固体.(1)该兴趣小组根据NaOH与CO2的反应,认为该白色固体的组成可能有以下几种情况:NaOH和Na2CO3、只有Na2CO3、只有NaHCO3、Na2CO3和NaHCO3.
(2)当通入标准状况下CO2的体积为2.24L时,该白色固体的组成为4 g NaOH和10.6 g Na2CO3(填写物质的化学式及对应质量).
①请设计实验方案进行实验验证.限选实验试剂:1mol•L-1 HCl溶液、1mol•L-1MgCl2溶液、0.5mol•L-1 BaCl2溶液、1mol•L-1Ba(OH)2溶液、甲基橙试液、酚酞试液.(步骤可不填满也可增加)
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: |
分析 (1)二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,二氧化碳恰好反应得到碳酸钠溶液,二氧化碳不足溶液中溶质为碳酸钠和氢氧化钠,当二氧化碳过量时,碳酸钠也会与二氧化碳反应;
(2)①要验证NaOH和Na2CO3同时存在,根据题中所给试剂,要首先利用中性溶液BaCl2检验出碳酸钠,并将碳酸根离子全部沉淀,再通过检验溶于的pH来确定是否含有NaOH;
②对NaOH和Na2CO3混合配成的溶液,当滴加盐酸时,先发生氢氧化钠与盐酸的中和反应,再发生碳酸钠与盐酸的反应生成碳酸氢钠和氯化钠,最后发生碳酸氢钠与盐酸反应才有二氧化碳气体生成,利用物质的量的关系并结合图象即可解答.
解答 解:(1)二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,二氧化碳恰好反应得到碳酸钠溶液,二氧化碳不足溶液中溶质为碳酸钠和氢氧化钠,当二氧化碳过量时,碳酸钠也会与二氧化碳反应,Na2CO3+CO2+H2O=2NaHCO3 ,可以得到溶液中的溶质为NaOH与CO2反应可生成Na2CO3或NaHCO3,或NaHCO3,所以白色固体可能为NaOH和Na2CO3、Na2CO3、NaHCO3、Na2CO3 和NaHCO3,
故答案为:NaOH和Na2CO3、Na2CO3、NaHCO3、Na2CO3 和NaHCO3;
(2)向300mL 1mol/L的NaOH溶液中通入一定量CO2,当通入标准状况下CO2的体积为2.24L时,
n(CO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,n(NaOH)=0.3L×1mol/L=0.3mol,
CO2+2NaOH=Na2CO3+H2O
1 2 1
0.1mol 0.2mol 0.1mol
此时氢氧化钠过量,得到溶液中Na2CO3质量=0.1×106g/mol=10.6g,NaOH的质量=(0.3mol-0.2mol)×40g/mol=4g,
①要验证NaOH和Na2CO3同时存在,根据题中所给试剂,要首先利用中性溶液BaCl2检验出碳酸钠,并将碳酸根离子全部沉淀,再通过检验溶于的pH来确定是否含有NaOH,
步骤1:取少量白色固体于试管中,加适量水溶解,再加0.5moL•L-1BaCl2溶液至过量,产生白色沉淀,说明固体中含有Na2CO3;
步骤2:过滤,取少量滤液(或:静置,用胶头滴管取上层清液少许)于试管中,再向试管中滴加1~2滴酚酞试液,溶液变红色,说明固体中含有NaOH,
故答案为:4 g NaOH和10.6 g Na2CO3
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量白色固体于试管中,加足量水溶解,再加足量0.5 mol•L-1 BaCl2溶液 | 产生白色沉淀,说明白色固体中含有Na2CO3 |
| 步骤2:过滤,取2 mL滤液于试管中,再向试管中滴加酚酞试液 | 溶液变红色,说明白色固体中含有NaOH |
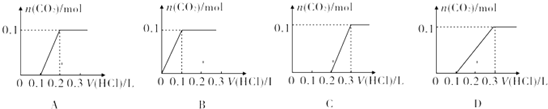
A、加入0.1L盐酸,n(HCl)=0.1L×1mol/L=0.1mol,0.1mol盐酸与氢氧化钠反应没有气体生成,再加入0.1molHCl,与0.1mol碳酸钠恰好反应生成碳酸氢钠,也没有气体生成,则图象与实际不符,故A错误;
B、先发生氢氧化钠与盐酸的中和反应,图象中开始反应即有气体生成,与反应不符,故B错误;
C、向NaOH和Na2CO3混合溶液中滴加盐酸时,首先和NaOH反应生成水和氯化钠,当滴入0.1L时,两者恰好反应完全;继续滴加时,盐酸和Na2CO3开始反应,首先发生HCl+Na2CO3=NaHCO3+NaCl,不放出气体,当再加入0.1L时,此步反应进行完全;继续滴加时,发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑,此时开始放出气体,再消耗0.1L盐酸,生成二氧化碳达最大,图象与实际相符合,故C正确;
D、因碳酸钠与盐酸的反应分步完成,则碳酸钠与盐酸先反应生成碳酸氢钠和氯化钠,此时没有气体生成,则图象与反应不符,故D错误;
故答案为:C.
点评 本题考查较为综合,以物质的制备实验为载体,综合考查实验的设计、物质的分离、提纯等知识,注意根据物质的性质设计实验方案,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA | |
| B. | 标准状况下,22.4LNO与CO2的混合气体中含有O原子数为3NA | |
| C. | 58.5 g的NaCl固体中含有NA个氯化钠分子 | |
| D. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA |

(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2气体和CO反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0 该反应的化学平衡常数表达式是K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$.已知平衡常数K与温度T的关系如表:
| T/℃ | 400 | 300 |
| 平衡常致K | K1 | K2 |
②下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)(正)=3v(H2)(逆)
c.容器内压强保持不变 d.混合气体的密度保持不变
③合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是BD(填字母).
A.采用较高温度(400℃~500℃) B.将生成的氨液化并及时从体系中分离出来
C.用铁触媒加快化学反应速率 D.采用较高压强(20MPa~50MPa)
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示,下列说法正确的是CD
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点N2O4的转化率:A<C
d.由状态B到状态A,可以用加热的方法.
| A. | 质谱法是测定有机物所含官能团的常用方法 | |
| B. | 红外光谱常用来测定有机物所含几种类型的氢原子 | |
| C. | 核磁共振氢谱可以区别乙醇与甲醚 | |
| D. | 红外光谱不能分别乙醇和甲醚 |
(1)甲烷(2)苯(3)聚乙烯(4)聚乙炔 (5)2-丁炔 (6)环己烷 (7)邻二甲苯 (8)苯乙烯.
| A. | (3)(4)(5)(8) | B. | (4)(5)(7)(8) | C. | (4)(5)(8) | D. | (3)(4)(5)(7)(8) |

