题目内容
14.T1温度下,反应2SO2(g)+O2(g)?2SO3(g);△H<0的平衡常数K=532.4.(1)该反应△S<0;升高温度,平衡常数减小(选填“增大”、“减小”或“不变”).
(2)T2温度下,2L容积固定的甲、乙两密闭容器中发生上述反应,测得平衡时有关数据如
表所列:
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 2molSO2、1molO2 | 4molSO3 |
| 平衡时n(SO3)/mol | 1 | m |
| 反应物的转化率 | α1 | α2 |
分析 (1)2SO2(g)+O2(g)?2SO3(g)△H<0,根据该反应为气体体积减小的放热反应判断熵变和平衡常数变化;
(2)因体积相同,将乙中的量极限转化后为甲中的2倍,则压强大于甲中的压强,三氧化硫的转化率减小;根据图表甲的数据计算T2时的平衡常数与T1平衡常数K=532.4比较判断温度大小.
解答 解:(1)2SO2(g)+O2(g)?2SO3(g)△H<0,该反应为气体体积减小的放热反应,所以△S<0,升高温度,平衡向吸热即逆反应方向移动,则反应常数减小;
故答案为:<;减小;
(2)因体积相同,将乙中的量极限转化后为甲中的2倍,则压强大于甲中的压强,减小了三氧化硫的转化率,则α1+α2<1;
根据甲开始2molSO2、1molO2,平衡时n(SO3)=1mol,所以平衡时剩余1molSO2、0.5molO2,生成n(SO3)=1mol,所以T2时的平衡常数=$\frac{(\frac{1}{2})^{2}}{(\frac{1}{2})^{2}•(\frac{0.5}{2})}$=4<T1平衡常数K=532.4,又升高温度,平衡常数减小,所以T1<T2,
故答案为:<;<.
点评 本题考查了化学平衡的计算,题目难度中等,明确化学平衡及其影响为解答关键,注意掌握化学平衡常数的表达式及应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
4.化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数数值如下,以下说法不正确的是( )
2NO(g)?N2(g)+O2(g) K1=1×1030;
2H2(g)+O2(g)?2H2O(g) K2=2×1081;
2CO2(g)?2CO(g)+O2(g) K3=4×10-92.
2NO(g)?N2(g)+O2(g) K1=1×1030;
2H2(g)+O2(g)?2H2O(g) K2=2×1081;
2CO2(g)?2CO(g)+O2(g) K3=4×10-92.
| A. | 升温时,三个反应的反应物的活化分子百分数均增加 | |
| B. | 常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 | |
| C. | 常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 | |
| D. | 降温时,三个反应的化学反应速率均减慢 |
9.中国环境监测数据显示,颗粒物(PM2.5等)为雾霾过程中影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
Ⅰ.改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气.
(1)煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为CO32-+H2S=HCO3-+HS-
(已知:H2S:Ka1=1.3×10-7,Ka2=7.1×10-15;H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11)
(2)现将不同量的CO(g)和H2O(g)分别通人到体积为2L的恒容密闭容器中发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H,得到两组数据
该反应的△H<0(填“<”或“>”);若在7500C时,另做一组实验,在2L的恒容密闭容器中加入lmol CO,3mo1H2O,2mo1CO2,5mol H2,则此时?正<?逆(填“<”,“>”,“=”).
(3)一定条件下,某密闭容器中已建立A(g)+B(g)?C(g)+D(g)△H>0的化学平衡,其时间速率图象如图1,下列选项中对于t1时刻采取的可能操作及其平衡移动情况判断正确的是A
A.减小压强,同时升高温度,平衡正向移动
B.增加A(g)浓度,同时降低温度,平衡不移动
C.保持容器温度压强不变通入稀有气体,平衡不移动
Ⅱ.压缩天然气(CNG)汽车的优点之一是利用催化技术将NOx转变成无毒的CO2和N2.
①CH4(g)+4NO(g)$\stackrel{催化剂}{?}$2N2(g)+CO2(g)+2H2O(g)△H1<0
②CH4(g)+2NO2(g)$\stackrel{催化剂}{?}$2N2(g)+CO2(g)+2H2O(g)△H2<0
(4)收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V (NO):V (NO2)=1:1.
(5)在不同条件下,NO的分解产物不同.在高压下,NO(即X)在40℃下分解生成两种化合物(即Y、Z),体系中各组分物质的量随时间变化曲线如图2所示.写出Y和Z的化学式:N2O、NO2
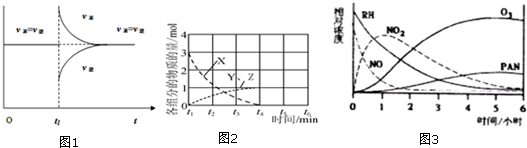
(6)某研究性学习小组,为研究光化学烟雾消长
规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),各种物质的相对浓度随时间的消失,记录于图3,根据图中数据,下列推论,最不合理的是D
A.NO的消失的速率比RH快
B.NO生成NO2
C.RH及NO2可以生成PAN及O3
D.O3生成PAN
Ⅰ.改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气.
(1)煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为CO32-+H2S=HCO3-+HS-
(已知:H2S:Ka1=1.3×10-7,Ka2=7.1×10-15;H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11)
(2)现将不同量的CO(g)和H2O(g)分别通人到体积为2L的恒容密闭容器中发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H,得到两组数据
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡 所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
(3)一定条件下,某密闭容器中已建立A(g)+B(g)?C(g)+D(g)△H>0的化学平衡,其时间速率图象如图1,下列选项中对于t1时刻采取的可能操作及其平衡移动情况判断正确的是A
A.减小压强,同时升高温度,平衡正向移动
B.增加A(g)浓度,同时降低温度,平衡不移动
C.保持容器温度压强不变通入稀有气体,平衡不移动
Ⅱ.压缩天然气(CNG)汽车的优点之一是利用催化技术将NOx转变成无毒的CO2和N2.
①CH4(g)+4NO(g)$\stackrel{催化剂}{?}$2N2(g)+CO2(g)+2H2O(g)△H1<0
②CH4(g)+2NO2(g)$\stackrel{催化剂}{?}$2N2(g)+CO2(g)+2H2O(g)△H2<0
(4)收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V (NO):V (NO2)=1:1.
(5)在不同条件下,NO的分解产物不同.在高压下,NO(即X)在40℃下分解生成两种化合物(即Y、Z),体系中各组分物质的量随时间变化曲线如图2所示.写出Y和Z的化学式:N2O、NO2
(6)某研究性学习小组,为研究光化学烟雾消长
规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),各种物质的相对浓度随时间的消失,记录于图3,根据图中数据,下列推论,最不合理的是D
A.NO的消失的速率比RH快
B.NO生成NO2
C.RH及NO2可以生成PAN及O3
D.O3生成PAN

6.下列说法符合化学事实的是( )
| A. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| B. | Na2SiO3水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 | |
| C. | 包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同 | |
| D. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 |
3.下列化学式中,只能用来表示一种物质的是( )
| A. | C2H4Cl2 | B. | C5H12 | C. | C | D. | C2H5Cl |
4.下列有关说法中正确的是( )
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| D. | 纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一 |

 .
.