题目内容
8.实验室要配制0.4mol/L的NaCl溶液250mL,请回答下列问题:①用天平准确称取NaCl固体5.9g g,放入小烧杯中,加适量蒸馏水溶解.
②将①所得的溶液转移至250 mL容量瓶中.
③用适量的蒸馏水洗涤烧杯和玻璃棒 2~3次,并把洗涤液小心的注入容量瓶中,轻轻振荡.
④继续向容量瓶中缓缓加入蒸馏水至液面距离刻度线1~2cm处,改用胶头滴管逐滴滴加蒸馏水至溶液的凹液面正好与刻度线相切.
⑤把容量瓶塞盖好,反复上下颠倒,充分摇匀.
分析 配制溶液的操作步骤:首先计算出需要的药品的质量,然后用托盘天平称量,后放入烧杯中溶解,同时用玻璃棒搅拌,待溶液冷却至室温后,用玻璃杯引流移液至250ml容量瓶,然后洗涤烧杯和玻璃棒2至3次,将洗涤液也注入容量瓶,然后向容量瓶中注水,至液面离刻度线1至2CM时,改用胶头滴管逐滴加入,至凹液面与刻度线相切,然后摇匀、装瓶.
①依据m=CVM计算溶质的质量;
②依据配制溶液体积选择合适的容量瓶;
③需洗涤溶解NaCl的烧杯、玻璃棒,否则会导致溶质的损失;
④定容用胶头滴管.
解答 解:①NaCl固体配制250mL 0.4mol/L的NaCl溶液,需要NaCl质量m=nM=CVM=0.4mol/L×0.25L×58.5g/mol=5.9g,
故答案为:5.9g
②配制250mL0.4mol/L的NaCl溶液,应选择250mL容量瓶,
故答案为:250;
③配制溶液,首先计算出需要的药品的质量,然后用托盘天平称量,后放入烧杯中溶解,同时用玻璃棒搅拌,少量溶质粘在溶解NaCl的烧杯、玻璃棒上,不进行洗涤,会导致溶质损耗,则溶液浓度偏小,所以需洗涤烧杯和玻璃棒,
故答案为:烧杯和玻璃棒;
④继续向容量瓶中缓缓加入蒸馏水至液面距离刻度线1~2cm处,改用胶头滴管进行定容,要逐滴滴加蒸馏水至溶液的凹液面正好与刻度线相切,
故答案为:胶头滴管.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和步骤是解题关键,题目难度不大.

练习册系列答案
相关题目
13.下列有关乙烯的说法,其中错误的是( )
| A. | 乙烯分子的双键中有一键较易断裂 | |
| B. | 烯分子里所有原子都在同一个平面上,且碳氢键之间的键角约为120° | |
| C. | 乙烯的化学性质比乙烷活泼 | |
| D. | 乙烯和环丙烷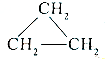 的分子组成符合通式CnH2n,因此它们属于同系物 的分子组成符合通式CnH2n,因此它们属于同系物 |
3.测定中和反应反应热的实验中,下列做法会导致反应热偏小的是( )
| A. | 用KOH溶液代替NaOH溶液 | B. | 用NaOH固体代替NaOH溶液 | ||
| C. | 反应物盐酸过量 | D. | 使用铜制搅拌棒搅拌 |
13.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于电解质的是BCD.
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为0.1 mol/L.
(3)配制上述“鲜花保鲜剂”用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少500mL容量瓶,胶头滴管(填写所缺仪器的名称).
(4)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容,
正确的操作顺序是⑤①④⑥③⑦②(填序号).
(5)若定容时俯视容量瓶刻度线,会使所配溶液浓度偏大(填偏大、偏小、不变).
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 3.48 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 1.58 | 158 |
| 硝酸银 | 0.02 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为0.1 mol/L.
(3)配制上述“鲜花保鲜剂”用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少500mL容量瓶,胶头滴管(填写所缺仪器的名称).
(4)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容,
正确的操作顺序是⑤①④⑥③⑦②(填序号).
(5)若定容时俯视容量瓶刻度线,会使所配溶液浓度偏大(填偏大、偏小、不变).
15.已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离的程度远大于第二步电离的程度,第二步电离的程度远大于第三步电离的程度….今有HA、H2B、H3C三种弱酸,根据“较强酸+较弱酸盐→较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
①HA+HC2-(少量)═A-+H2C-;
②H2B(少量)+2A-═B2-+2HA;
③H2B(少量)+H2C-═HB-+H3C.
下列离子方程式不能发生的是( )
①HA+HC2-(少量)═A-+H2C-;
②H2B(少量)+2A-═B2-+2HA;
③H2B(少量)+H2C-═HB-+H3C.
下列离子方程式不能发生的是( )
| A. | HB-+A-═HA+B2- | B. | H3C+3A-═3HA+C3- | ||
| C. | H3C+B2-═HB-+H2C- | D. | H3C+3OH-═3H2O+C3- |
 23个水分子中,含分子数最多的是(填序号,下同)________,含原子数最多的是________,质量最大的是________,体积最小的是______。
23个水分子中,含分子数最多的是(填序号,下同)________,含原子数最多的是________,质量最大的是________,体积最小的是______。 O4)3溶液中含有Fe3+ m g,则溶液中SO42﹣的物质的量浓度为
O4)3溶液中含有Fe3+ m g,则溶液中SO42﹣的物质的量浓度为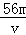 mol/L B.
mol/L B.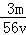 mol/L C.
mol/L C.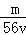 mol/L D.
mol/L D. mol/L
mol/L