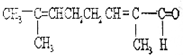题目内容
18.按体积比2:3混合的N2与CO2 112.8g在标准状况下体积为( )| A. | 22.4L | B. | 44.8L | C. | 67.2L | D. | 89.6L |
分析 体积之比等于物质的量之比,令氮气的物质的量为2xmol,则二氧化碳为3xmol,根据混合气体的质量,求算x的值,再根据V=nVm计算混合气体标准状况下体积.
解答 解:体积之比等于物质的量之比,令氮气的物质的量为2xmol,则二氧化碳为3xmol,所以:
2xmol×28g/mol+3xmol×44g/mol=112.8g,
解得x=0.6mol,则氮气的物质的量为n=2x=1.2mol,二氧化碳的物质的量n=3x=1.8mol.
则混合气体的物质的量共有1.2mol+1.8mol=3mol,则在标况下的体积V=nVm=3mol×22.4L/mol=67.2L.
故选C.
点评 本题考查了混合气体的物质的量和体积等有关计算,难度不大,注意理清解题思路,在同温同压下,气体体积之比等于物质的量之比.

练习册系列答案
相关题目
9.下列关于新制氯水的叙述不正确的是( )
| A. | 呈黄绿色,说明氯水中有Cl2 | |
| B. | 加入Na2CO3溶液产生气体,说明氯水有酸性 | |
| C. | 加入红色纸条,红色纸条褪色,说明氯水有漂白性 | |
| D. | 滴入石蕊溶液,溶液变成红色并保持不变,说明氯水有酸性 |
3.X、Y是浓度均为0.1mol/L的溶液中的某一种:①混有少量盐酸的MgSO4溶液 ②Al2(SO4)3溶液 ③明矾溶液 ④Ba(OH)2溶液 ⑤NaOH溶液.现向溶液X中逐滴加入溶液Y.得到的沉淀量与所加Y溶液的体积的关系的部分图象如图所示.则符合该图象的X、Y的组合共有( )

| A. | 4种 | B. | 5种 | C. | 6种 | D. | 8种 |
7.下列有关氧化剂还原反应的判断正确的是( )
| A. | 在反应Cl2+2NaOH═NaCl+NaClO+H2O中,Cl2是氧化剂,NaOH是还原剂 | |
| B. | 在反应MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,HCl是氧化剂,MnO2是还原剂 | |
| C. | 在反应NaH+H2O═NaOH+H2↑中,H2既是氧化物又是还原产物 | |
| D. | 在反应H2S+H2SO4═S↓+SO2↑+2H2O中SO2是氧化产物,S是还原产物 |
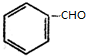 +H2(足量):
+H2(足量):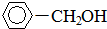 .
.