题目内容
3.X、Y是浓度均为0.1mol/L的溶液中的某一种:①混有少量盐酸的MgSO4溶液 ②Al2(SO4)3溶液 ③明矾溶液 ④Ba(OH)2溶液 ⑤NaOH溶液.现向溶液X中逐滴加入溶液Y.得到的沉淀量与所加Y溶液的体积的关系的部分图象如图所示.则符合该图象的X、Y的组合共有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 8种 |
分析 根据图象可知,加入Y就立即生成沉淀,最终沉淀没有全部溶解,据此分析;
解答 解:当Y为混有少量盐酸的MgSO4溶液,则溶液X可以为Ba(OH)2溶液,当加入Y立即生成硫酸钡沉淀;
当Y为Al2(SO4)3溶液,则溶液X可以为Ba(OH)2溶液,当加入Y立即生成硫酸钡沉淀;
当Y为明矾溶液,则溶液X可以为Ba(OH)2溶液,当加入Y立即生成硫酸钡沉淀;
当Y为Ba(OH)2溶液,则溶液X可以为混有少量盐酸的MgSO4溶液或者Al2(SO4)3溶液或者明矾溶液,当加入Y都会立即生成硫酸钡沉淀;
当Y为NaOH溶液,没有符合条件;
所以一共6种;
故选:C.
点评 本题以反应图象形式考查元素化合物性质,难度中等,根据清楚图象反应过程是解题关键.

练习册系列答案
相关题目
13.下列说法正确的是( )
| A. |  表示在其他条件不变时,2SO2 (g)+02 (g)?2S03 (g)转化关系中,纵坐标表示02的转化率 | |
| B. |  表示用0.1mol/L NaOH溶液分别滴定等浓度、等体积的盐酸和醋酸,其中实线为滴定醋酸的曲线 | |
| C. | 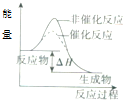 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| D. | 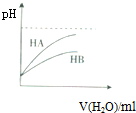 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则酸性HA<HB |
14.下列实验“操作和现象”与“结论”的对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 常温下将铝片放入浓硝酸中,无明显变化 | Al与浓硝酸不反应 |
| B | 向0.1mol•L-1 Na2CO3溶液中,滴加2滴酚酞,溶液显浅红色,微热,红色加深 | 盐类水解是吸热反应 |
| C | 向FeCl3溶液中加入足量的铜粉,充分反应后,静止,取上层清液滴加几滴KSCN溶液,溶液不变红色 | 氧化性:Cu 2+>Fe3+ |
| D | 向2mL 1mol•L-1 NaOH溶液中先加入3滴1mol•L-1 MgCl2溶液,再加入3滴1mol•L-1FeCl3溶液,沉淀由白色变成红褐色 | Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 |
| A. | A | B. | B | C. | C | D. | D |
11.由乙醛、乙醇、丁醇三种物质组成的混合物0.1mol,完全燃烧后,将所得气体先通过浓硫酸,然后再通过盛有碱石灰的干燥管,测得浓硫酸的质量增加了5.4克.则原混合物中乙醛、乙醇、丁醇的物质的量之比为( )
| A. | 2:3:1 | B. | 1:2:3 | C. | 4:3:2 | D. | 3:2:1 |
18.按体积比2:3混合的N2与CO2 112.8g在标准状况下体积为( )
| A. | 22.4L | B. | 44.8L | C. | 67.2L | D. | 89.6L |
8.镓、铝为同族元素,性质相似,现将一块镓铝合金完全溶于烧碱溶液中得到溶液X.已知:
①氢氧化镓的电离方程式是H++H2O+GaO2-?Ga(OH)3?Ga3++3OH-;
②镓与烧碱溶液反应的离子方程式是2Ga+2H2O+2OH-=2GaO2-+3H2↑;
③往X溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
| Al(OH)3 | Ga(OH)3 | |
| 酸式电离常数Ka | 2×10-11 | 1×10-7 |
| 碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
②镓与烧碱溶液反应的离子方程式是2Ga+2H2O+2OH-=2GaO2-+3H2↑;
③往X溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
15.常温时,浓度为0.01mol•L-1的稀盐酸用蒸馏水稀释108倍,则稀释后溶液的pH约为( )
| A. | 2 | B. | 7 | C. | 10 | D. | 12 |