题目内容
6.表为元素周期表的局部,A、B、C、D为周期表中短周期元素,已知A原子最外电子层上的电子数是其次外层的一半.据此判断下列正确的是( )| B | D | ||
| A | C |
| A. | A位于第2周期1A族 | B. | B的最高价氧化物的水化物是弱酸 | ||
| C. | 原子半径A>C>B>D | D. | 气态氢化物的热稳定性B>D>C>A |
分析 根据元素在周期表中的相对位置可知,A是第三周期元素.A原子最外电子层上的电子数是其次外层的一半,则A是Si元素,因此B是氮元素,C是S元素,D是F元素,结合元素在周期表中的位置以及元素周期率知识解答该题.
解答 解:根据元素在周期表中的相对位置可知,A是第三周期元素.A原子最外电子层上的电子数是其次外层的一半,则A是Si元素,因此B是氮元素,C是S元素,D是F元素.
A.A是Si元素,位于周期表第三周期,故A错误;
B.B为N元素,对应的.最高价氧化物的水化物是硝酸,为强酸,故B错误;
C.同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径原子半径A>C>B>D,故C正确;
D.非金属性越强,氢化物的稳定性越强,则气态氢化物的热稳定性D>B>C>A,故D错误.
故选C.
点评 本题考查结构位置性质关系、元素周期表、元素周期律等,为高考常见题型,侧重于学生的分析能力的考查,比较基础,注意整体把握元素周期表的结构与元素周期律.

练习册系列答案
相关题目
20.下列反应中,二氧化碳作氧化剂的是( )
| A. | Ca(OH)2+CO2═CaCO3↓+H2O | B. | 2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2 | ||
| C. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO | D. | CO2+H2O═H2CO3 |
16.某有机物可用于合成一种常见药物达菲,其结构简式如图,下列关于该有机物的说法正确的是( )

| A. | 分子式为C7H6O5 | |
| B. | 可发生加成和取代反应 | |
| C. | 分子中含有两种官能团 | |
| D. | 在水溶液中羧基和羟基均能电离出H+ |
2.下列关于四种粒子的结构示意图的说法中正确的是( )
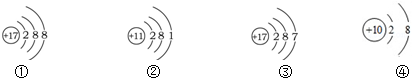
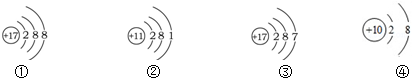
| A. | ①③属于同种元素 | |
| B. | ①属于离子,离子符号为Cl-1 | |
| C. | ①④的化学性质相似 | |
| D. | ②表示的元素在化合物中通常显-1价 |
11.下述叙述中正确的是( )
| A. | 标准状况下,11.2L四氯化碳所含分子数为0.5×6.02×1023个 | |
| B. | 36.5g氯化氢中含有6.02×1023个氢离子 | |
| C. | 7.8gNa2O2与足量的水反应,转移的电子数为0.2×6.02×1023 | |
| D. | 标准状况下,2.24L CO2和SO2混合物中所含有的原子数为0.3×6.02×1023 |
18.下列氯化物中,能直接利用金属与稀盐酸的反应得到的是( )
| A. | FeCl3 | B. | CuCl2 | C. | AgCl | D. | FeCl2 |
15.容量瓶上需要标有:①温度,②浓度,③容量,④压强,⑤刻度线,⑥碱式或酸式六项中的( )
| A. | ①③⑤ | B. | ②④⑥ | C. | ③⑤⑥ | D. | ①②③ |
16.有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如表所示:
由此判断:
(1)溶液中肯定存在的离子是NO3-、SO42- Mg2+、Al3+,
溶液中肯定不存在的离子是I-、Ba2+、Fe2+、HCO3-;
溶液中可能存在的离子是K+、Cl-.
(2)请设计实验验证原溶液中可能存在的阴离子的方法(写明操作、现象、结论)
取少许原溶液于试管中,先加入过量的硝酸钡溶液,再往上层清液中滴加硝酸银溶液,若出现白色沉淀则说明含有Cl-.
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴甲基橙 | 溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| (4)取(3)中上层清液,加AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
(1)溶液中肯定存在的离子是NO3-、SO42- Mg2+、Al3+,
溶液中肯定不存在的离子是I-、Ba2+、Fe2+、HCO3-;
溶液中可能存在的离子是K+、Cl-.
(2)请设计实验验证原溶液中可能存在的阴离子的方法(写明操作、现象、结论)
取少许原溶液于试管中,先加入过量的硝酸钡溶液,再往上层清液中滴加硝酸银溶液,若出现白色沉淀则说明含有Cl-.