题目内容
20.下列反应中,二氧化碳作氧化剂的是( )| A. | Ca(OH)2+CO2═CaCO3↓+H2O | B. | 2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2 | ||
| C. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO | D. | CO2+H2O═H2CO3 |
分析 反应中,二氧化碳作氧化剂,则二氧化碳中C元素的化合价降低,据此分析.
解答 解:A.Ca(OH)2+CO2═CaCO3↓+H2O反应中,没有元素化合价的变化,不是氧化还原反应,故A错误;
B.2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2中C元素的化合价升高,则C为还原剂,CO2为氧化产物,故B错误;
C.CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO反应,CO2中C元素的化合价降低,则CO2为氧化剂,故C正确;
D.CO2+H2O═H2CO3反应中,没有元素化合价的变化,不是氧化还原反应,故D错误.
故选C.
点评 本题考查氧化还原反应知识,侧重于基本概念的考查,难度不大,注意从元素化合价的角度认识物质的性质以及相关概念.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
8..下列仪器中,不能作为反应容器的是( )
| A. | 试管 | B. | 烧杯 | C. | 容量瓶 | D. | 锥形瓶 |
15.下列实验操作或对实验事实的描述中正确的是( )
| A. | 燃着的酒精灯不慎碰翻失火,可立即用湿布盖灭 | |
| B. | 配制溶液的容量瓶要用欲配制的溶液润洗过 | |
| C. | 配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 用托盘天平称量时,所称药品均可放在纸上,并置于天平的左盘 |
5.配制NaOH溶液时,下列操作情况会使结果偏高的是( )
| A. | 没有洗涤烧杯和玻璃棒 | |
| B. | 使用容量瓶之前发现其内有少量蒸馏水残留 | |
| C. | 定容时,俯视容量瓶刻度线观察液面 | |
| D. | 定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容 |
12.下列离子方程式书写正确的是( )
| A. | 铜片放入稀硫酸中:Cu+2H+=Cu2++H2↑ | |
| B. | 将少量NaOH溶液加入NH4HCO3溶液中:OH-+HCO3-=CO32-+H2O | |
| C. | 向NaHCO3溶液中加入少量Ca(OH)2:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| D. | Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
6.表为元素周期表的局部,A、B、C、D为周期表中短周期元素,已知A原子最外电子层上的电子数是其次外层的一半.据此判断下列正确的是( )
| B | D | ||
| A | C |
| A. | A位于第2周期1A族 | B. | B的最高价氧化物的水化物是弱酸 | ||
| C. | 原子半径A>C>B>D | D. | 气态氢化物的热稳定性B>D>C>A |
7.常温下,柠檬水溶液的pH是3,其中的c(OH-)是( )
| A. | 10-11mol/L | B. | 10-3mol/L | C. | 10-7mol/L | D. | 0.1 mol/L |
 B.
B.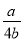 C.
C. mol-1 D.
mol-1 D.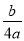 mol-1
mol-1 4NO+6H2O
4NO+6H2O