题目内容
10.下列物质的水溶液因水解呈碱性的是( )| A. | Na2CO3 | B. | NaOH | C. | HCl | D. | AlCl3 |
分析 物质的水溶液因水解呈碱性的是强碱弱酸盐,据此分析.
解答 解:A.碳酸钠是强碱弱酸盐,水解溶液显碱性,CO32-+H2O?HCO3-+OH-,故A正确;
B.NaOH是强碱,在水中能电离出大量的氢氧根,故是电离显碱性,故B错误;
C.氯化氢是强酸,在溶液中完全电离溶液显酸性,故C错误;
D.氯化铝是强酸弱碱盐,在溶液中能电离为铝离子水解溶液呈酸性,Al3++3H2O?Al(OH)3+3H+,氯离子不水解,故D错误.
故选A.
点评 本题考查了盐类的水解和电解质的电离,难度不大,应注意的是碱一定显碱性,但显碱性的不一定是碱.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
20.下列过程或现象与盐类水解无关的是( )
| A. | 可用碳酸钠与醋酸溶液制取少量二氧化碳 | |
| B. | 将NaHCO2与Al2(SO4)3两种溶液配制泡沫灭火剂 | |
| C. | 热的纯碱溶液的去污能力更强 | |
| D. | 实验室用饱和的FeCl3溶液制取氢氧化铁胶体 |
1.已知反应:2H2O(g)$?_{光照}^{Cu_{2}O}$2H2(g)+O2(g)△H=+484kJ•mol-1.某温度下,在4L密闭容器中加入纳米级Cu2O并通入0.2mol H2O(g),记录不同时间产生O2的物质的量如表:
下列说法正确的是( )
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0020 | 0.0032 | 0.0040 | 0.0040 |
| A. | 前20min的反应速率v(H2O)=2.5×10-5mol•L-1•min-1 | |
| B. | 达平衡时,至少需要从外界吸收的能量为0.968kJ | |
| C. | 增大c(H2O),可以提高水的分解率 | |
| D. | 使用纳米级Cu2O颗粒是为了提高催化效果 |
18.如图所示的电化学装置中,电极I为Al,其他电极均为Cu,则下列说法正确的是( )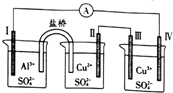

| A. | 电子流向:电极Ⅳ→(A)→电极I | |
| B. | 电极Ⅲ的电极反应:2H2O一4e一=4H++O2↑ | |
| C. | 电极Ⅱ的质量减少,电极Ⅲ的质量增加 | |
| D. | 三个烧杯中的SO42-浓度都始终保持不变 |
5.下列物质中属于盐的是( )
| A. | MgO | B. | H2SO4 | C. | NaOH | D. | KNO3 |
15.下列物质的制备,不符合工业生产实际的是( )
| A. | 工业上用电解熔融氯化镁制单质镁 | |
| B. | 工业上用电解饱和食盐水制氯气 | |
| C. | 工业上用二氧化硅在高温下与焦炭反应制得高纯度的硅 | |
| D. | 工业上炼铁时,常用石灰石除去铁矿石中的SiO2 |
2.下列离子方程式正确的是( )
| A. | 将氯气通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 铁与FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 硫酸溶液与氯化钡溶液混合:Ba2++SO42-═BaSO4↓ |
19.下列叙述正确的是( )
| A. | 0.5mol•L-1CuCl2溶液含有3.01×1023个Cu2+ | |
| B. | 28g聚乙烯分子含有的碳原子数为 NA | |
| C. | 0.2mol PCl5分子中,键数目为NA | |
| D. | 标准状况下,3.36L H2O含有9.03×1023个H2O分子 |