题目内容
19.下列叙述正确的是( )| A. | 0.5mol•L-1CuCl2溶液含有3.01×1023个Cu2+ | |
| B. | 28g聚乙烯分子含有的碳原子数为 NA | |
| C. | 0.2mol PCl5分子中,键数目为NA | |
| D. | 标准状况下,3.36L H2O含有9.03×1023个H2O分子 |
分析 A.缺少溶液体积,无法计算溶液中含有铜离子的物质的量;
B.聚乙烯的最简式为CH2,根据最简式进行计算含有碳原子数;
C.0.2mol PCl5分子中含有1mol共价键;
D.标准状况下,水的状态不是气体,不能使用标准状况下的气体摩尔体积计算.
解答 解:A.没有告诉0.5mol•L-1CuCl2溶液的体积,无法计算溶液中含有铜离子的物质的量,故A错误;
B.28g聚乙烯分子中含有28g最简式CH2,含有最简式的物质的量为:$\frac{28g}{14g/mol}$=2mol,含有2mol碳原子,含有的碳原子数为2NA,故B错误;
C.0.2mol PCl5分子中含有共价键的物质的量为:0.2mol×5=1mol,含有的键数目为NA,故C正确;
D.标准状况下,水不是气体,不能使用标准状况下的气体摩尔体积计算水的物质的量,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
9.下列离子方程式正确的是( )
| A. | NaHCO3溶液呈碱性的原因:HCO3-+H2O?CO32-+H3O+ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至沉淀质量最大:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | 氢氧化铝溶于醋酸溶液:Al(OH)3+3H+═Al3++3H2O | |
| D. | 氯化铝溶液中加入过量氨水Al3++4OH-═AlO2-+2H2O |
10.下列物质的水溶液因水解呈碱性的是( )
| A. | Na2CO3 | B. | NaOH | C. | HCl | D. | AlCl3 |
7.下列说法不正确的是( )
| A. | 配制一定物质的量浓度的溶液,向容量瓶加水至液面离刻度线1~2 cm时,改用胶头滴管定容 | |
| B. | 向某溶液中先加入Ba(NO3)2溶液,再加入足量的HNO3溶液,产生白色沉淀,则该溶液中一定含有SO42- | |
| C. | 分液操作时,将下层液体先放出,然后关闭旋塞,将上层液体从上口倒出 | |
| D. | 将油脂与氢氧化钠溶液混合充分反应后,再加入热的饱和食盐水,则可析出肥皂的主要成分 |
5.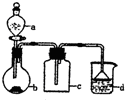 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是
( )
 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是| 选项 | A中的物质 | b中的物质 | c中的物质 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO | H2O |
| D | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 酒精和水 | B. | 碘和酒精 | C. | 水和CCl4 | D. | 汽油和植物油 |