题目内容
下列有关化学用语表示不正确的是( )
A、氧的原子结构示意图: |
B、Na2O2的电子式: |
| C、HClO的结构式:H-O-Cl |
| D、中子数为16的硫离子:S2- |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氧原子的核电荷数=核外电子总数=8,最外层为6个电子;
B.过氧化钠为离子化合物,钠离子和过氧根离子都需要标出所带电荷,过氧根离子还需要标出原子的最外层电子;
C.次氯酸中存在1个氧氯将和一个氧氢键,用短线表示出所有共用电子对即为结构式;
D.硫离子的核电荷数为16,质量数=质子数+中子数,元素符号的左上角表示质量数.
B.过氧化钠为离子化合物,钠离子和过氧根离子都需要标出所带电荷,过氧根离子还需要标出原子的最外层电子;
C.次氯酸中存在1个氧氯将和一个氧氢键,用短线表示出所有共用电子对即为结构式;
D.硫离子的核电荷数为16,质量数=质子数+中子数,元素符号的左上角表示质量数.
解答:
解:A.氧原子的核电荷数、最外层电子式都为8,最外层为6个电子,氧原子正确的结构示意图为: ,故A错误;
,故A错误;
B.Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子,电子式为: ,故B正确;
,故B正确;
C.次氯酸的电子式为: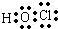 ,将所有共用电子对换成短线即为结构式,次氯酸的结构式为:H-O-Cl,故C正确;
,将所有共用电子对换成短线即为结构式,次氯酸的结构式为:H-O-Cl,故C正确;
D.中子数为16的硫离子的质量数为32,该离子可以表示为:1632S2-,故错误;
故选AD.
 ,故A错误;
,故A错误;B.Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子,电子式为:
 ,故B正确;
,故B正确;C.次氯酸的电子式为:
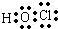 ,将所有共用电子对换成短线即为结构式,次氯酸的结构式为:H-O-Cl,故C正确;
,将所有共用电子对换成短线即为结构式,次氯酸的结构式为:H-O-Cl,故C正确;D.中子数为16的硫离子的质量数为32,该离子可以表示为:1632S2-,故错误;
故选AD.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、结构式、元素符号、原子结构示意图的书写原则,明确离子结构示意图与原子结构示意图、电子式与分子式、结构式、离子化合物与共价化合物的电子式的区别.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
某学生做完实验后,采用下列方法清洗所用仪器下列对以上操作的判断.正确的是( )
①用浓氨水清洗做过银镜反应后的试管
②用酒精清洗做过碘升华的烧杯
③用浓盐酸清洗做过高锰酸钾分解实验的试管
④用盐酸清洗长期存放三氯化铁溶液的试剂瓶
⑤用氢氧化钠溶液清洗盛过苯酚的试管
⑥用热氢氧化钠的浓溶液清洗沾有硫磺的试管.
①用浓氨水清洗做过银镜反应后的试管
②用酒精清洗做过碘升华的烧杯
③用浓盐酸清洗做过高锰酸钾分解实验的试管
④用盐酸清洗长期存放三氯化铁溶液的试剂瓶
⑤用氢氧化钠溶液清洗盛过苯酚的试管
⑥用热氢氧化钠的浓溶液清洗沾有硫磺的试管.
| A、除①外都对 | B、除⑥外都对 |
| C、④⑤不对 | D、全都正确 |
已知在室温时纯水中存在电离平衡:H2O?H++OH-.下列叙述正确的是( )
| A、同浓度、同体积的NaOH和氨水溶液中,水的电离程度相同 |
| B、升高温度,水的电离程度增大,c(H+)增大,pH<7,所以溶液显酸性 |
| C、向水中加入氨水,平衡逆向移动,水的电离受到抑制,所以c(OH-)降低 |
| D、向水中加入少量硫酸,c(H+)增大 |
下列有关物质分类或归纳正确的是( )
①电解质:明矾、冰醋酸、氯化银、纯碱
②同素异形体:金刚石、石墨;C60、C70
③混合物:盐酸、漂白粉、水玻璃、水银
④化合物:BaCl2、Ca(OH)2、HNO3、HT.
①电解质:明矾、冰醋酸、氯化银、纯碱
②同素异形体:金刚石、石墨;C60、C70
③混合物:盐酸、漂白粉、水玻璃、水银
④化合物:BaCl2、Ca(OH)2、HNO3、HT.
| A、①② | B、②③ | C、③④ | D、②④ |
下列说法错误的是( )
| A、化学反应中的能量变化都表现为热量变化 |
| B、需要加热才能发生的反应不一定是吸热反应 |
| C、向醋酸钠溶液中滴入酚酞试液,加热后若溶液红色加深,则说明盐类水解是吸热的 |
| D、反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
(B做)有一空瓶的质量为20g,问该瓶中充入氧气后的质量为36g,在相同的条件下充入某气体,其质量为34g,则该气体的摩尔质量为( )
| A、44g/mol |
| B、28g/mol |
| C、64g/mol |
| D、32g/mol |