题目内容
17.有关物质的转化关系如图所示(部分物质和条件已略去).A是日常生活中一种常见的调味剂,B是最常见的液体,G是一种常见金属单质,H、I、J、K都是含有G元素的化合物,I 的摩尔质量为102g•mol-1,K是一种难溶于水的白色胶状沉淀.请回答下列问题: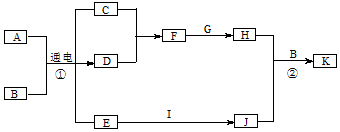
(1)I的化学式为Al2O3.
(2)F的电子式为
 .
.(3)写出①反应的离子方程式:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH-.
(4)写出②反应的化学方程式:3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+3NaCl.
分析 A是日常生活中一种常见的调味剂,应为NaCl,B是最常见的液体,应为2H2O,电解NaCl溶液,可生成Cl2、H2、NaOH,K是一种难溶于水的白色胶状沉淀,常见为Al(OH)3,则G为Al,由转化关系可知F为HCl,H为AlCl3,E为NaOH,I 的摩尔质量为102g•mol-1,为Al2O3,J为NaAlO2,以此解答该题.
解答 解:(1)由以上分析可知I为Al2O3,故答案为:Al2O3;
(2)F为HCl,为共价化合物,电子式为

(3)反应①为电解NaCl溶液的反应,离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH-,
故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH-;
(4)反应②为NaAlO2和AlCl3的反应,生成氢氧化铝,化学方程式为3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+3NaCl,
故答案为:3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+3NaCl.
点评 本题考查了物质转化关系分析判断,为高考常见题型,侧重考查学生的分析能力,题目主要涉及铝及其化合物性质,氯气及其化合物性质的分析应用,注意反应特征的理解应用是解题关键,题目难度中等.

练习册系列答案
相关题目
7.某温度下,对可逆反应:2X(g)+Y(g)?Z(g)+W(s)△H>0,则下列叙述正确的是( )
| A. | 加入少量W,逆反应速率增大 | |
| B. | 升高温度时,正反应速率增大,逆反应速率减小 | |
| C. | 压强不变,充入与反应体系不反应的N2,Z的物质的量减少 | |
| D. | 平衡后加入X,上述反应的△H增大 |
8.${\;}_{235}^{92}$U是重要的工业原料,铀浓缩一直为国际社会关注.下列说法正确的是( )
| A. | ${\;}_{235}^{92}$U原子核中含有 92 个中子 | |
| B. | ${\;}_{235}^{92}$U原子核外有 143 个电子 | |
| C. | ${\;}_{235}^{92}$U 与 ${\;}_{92}^{238}$U 互为同位素 | |
| D. | ${\;}_{235}^{92}$U与${\;}_{92}^{238}$U 同一核素 |
12.下列过程只涉及物理变化的是( )
| A. | 冰雪消融 | B. | 食物腐败 | C. | 钻木取火 | D. | 蜡炬成灰 |
2.下列图示实验能达到实验目的是( )
| A. | 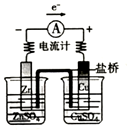 探究原电池原理 | B. | 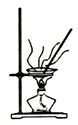 制备无水氯化铁 | ||
| C. | 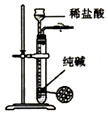 制取少量纯净的CO2气体 | D. |  收集氨气 |
9.日常生活中常用到加碘食盐和铁强化酱油,这里的碘和铁指的是( )
| A. | 元素 | B. | 单质 | C. | 原子 | D. | 分子 |
6.下列离子方程式书写正确的是( )
| A. | 醋酸和氨水反应:H++OH-=H2O | |
| B. | 等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O | |
| C. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2CIO-+CO2+H2O=CaCO3+2HCIO | |
| D. | 苯酚钠溶液中通入少量二氧化碳:2C6H6O-+CO2+H2O→2C6H5OH+CO32- |
2.实验室用稀硝酸与铜反应制备硝酸铜晶体及NO气体,需经过铜与稀硝酸反应、收集NO、尾气处理、制取硝酸铜晶体四个步骤,下列图示装置和原理能达到实验目的是( )
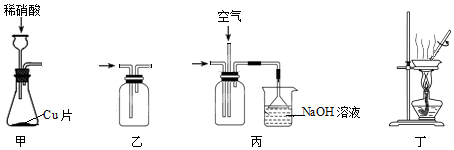

| A. | 用装置甲制取Cu(NO3)2和NO | B. | 用装置乙收集NO | ||
| C. | 用装置丙吸收尾气 | D. | 用装置丁蒸发结晶制Cu(NO3)2•3H2O |
