题目内容
4.下列设计的实验方案能达到实验目的是( )| A. | 检验蔗糖是否水解:蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察现象 | |
| B. | 检验溶液中是否含有NH4+:取少量待检验溶液,向其中加入浓NaOH溶液加热,再用湿润的红色石蕊试纸放置试管口,观察现象 | |
| C. | 提纯含有少量苯酚的苯:向含有少量苯酚的苯加入过量浓溴水,振荡后静置过滤,除去三溴苯酚沉淀 | |
| D. | 浸有KMnO4(H+)溶液的滤纸中滴加SO2水溶液,滤纸褪色,说明SO2具有漂白性 |
分析 A.葡萄糖和银氨溶液发生银镜反应必须在碱性条件下;
B.NH4+和NaOH反应生成一水合氨,一水合氨在加热条件下分解生成氨气,氨气能使湿润的红色石蕊试纸变蓝色;
C.苯酚和溴反应生成的三溴苯酚沉淀、苯、苯酚能互溶;
D.二氧化硫具有还原性,能被强氧化性物质氧化.
解答 解:A.葡萄糖和银氨溶液发生银镜反应必须在碱性条件下,所以在加入银氨溶液之前必须加入少量NaOH溶液,中和未反应的稀硫酸,否则实验不成功,故A错误;
B.NH4+和NaOH反应生成一水合氨,一水合氨在加热条件下分解生成氨气,氨气能使湿润的红色石蕊试纸变蓝色,该实验能检验铵根离子,故B正确;
C.苯酚和溴反应生成的三溴苯酚沉淀、苯、苯酚能互溶,应该用NaOH溶液和苯酚反应,然后采用分液方法分离提纯,故C错误;
D.二氧化硫具有还原性,能被强氧化性物质高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,该实验体现二氧化硫的还原性,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及二氧化硫的性质、除杂、离子检验等知识点,明确实验原理及物质性质是解本题关键,注意除杂时要除去杂质且不能引进新的杂质,操作要简便,注意二氧化硫还原性和漂白性的区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列各电子式中正确的是( )
| A. | 氯原子  | B. | 氟原子  | C. | 溴化钡  | D. | 硫化钾  |
12.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在pH=1的溶液中:K+、Na+、SO42-、HCO3- | |
| B. | 在0.1 mol•L-1 Na2CO3溶液中:Al3+、K+、NO3-、SO42- | |
| C. | 在0.1 mol•L-1 FeCl3溶液中:K+、NH4+、I-、SCN- | |
| D. | 在pH=12的溶液中:K+、Na+、ClO-、NO3- |
19.下列说法中正确的是( )
| A. | 所有的原子核内都有质子和中子 | |
| B. | (H+)实质上是一个裸露的质子 | |
| C. | 核外电子排布相同的微粒,其化学性质也相同 | |
| D. | 非金属元素原子最外层电子数都大于4 |
16.某芳香族有机物的分子式为C8H6O2,它的分子(除苯环外不含其他环)中可能有( )
| A. | 两个羟基 | B. | 一个酯基 | C. | 两个醛基 | D. | 一个羧基 |
13.下列叙述正确的是( )
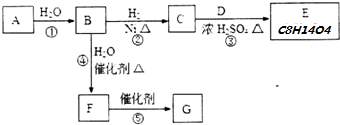
| A. | CO2的电子式为 | |
| B. | 所有的主族元素的简单离子的化合价与其族序数相等 | |
| C. | NH4Cl晶体中,既含有离子键,又含有共价键 | |
| D. | 下列物质均为极性分子:H2O、NH3、CCl4 |
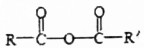 $\stackrel{H_{2}O}{→}$RCOOH+R′COOH(其中R,R′是烃基)
$\stackrel{H_{2}O}{→}$RCOOH+R′COOH(其中R,R′是烃基)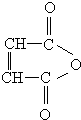 ,B中所含官能团的名称是羧基、碳碳双键;③和⑤的反应类型分别是取代反应、缩聚反应.
,B中所含官能团的名称是羧基、碳碳双键;③和⑤的反应类型分别是取代反应、缩聚反应.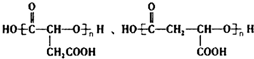 .
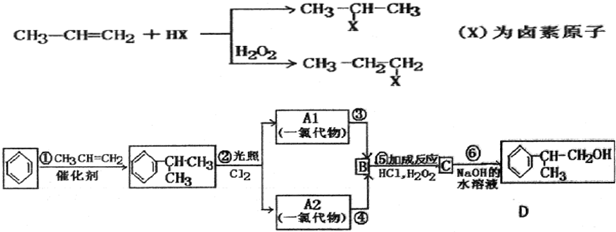
.
 ;
;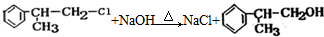 ;
;