题目内容
5.乙醇是重要的化工原料,下列说法正确的有( )| A. | 乙醇催化氧化可制备乙醛 | B. | 乙醇与H2反应可制备乙烷 | ||
| C. | 乙醇与金属钠反应可制备乙醇钠 | D. | 乙醇与乙酸反应可制备乙酸乙酯 |
分析 A.乙醇催化氧化生成乙醛和水;
B.乙醇与氢气不反应;
C.乙醇含有羟基;
D.醇与酸在催化剂条件下能够生成酯.
解答 解:A.乙醇催化氧化生成乙醛和水,所以乙醇催化氧化可制备乙醛,故A正确;
B.乙醇与氢气不反应,故B错误;
C.乙醇含有羟基,能够与钠发生置换反应生成乙醇钠和氢气,故C正确;
D.乙醇与乙酸反应可制备乙酸乙酯,故D正确;
故选:ACD.
点评 本题考查了物质的性质,明确乙醇分子结构特点,熟悉其化学性质是解题关键,题目难度不大.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
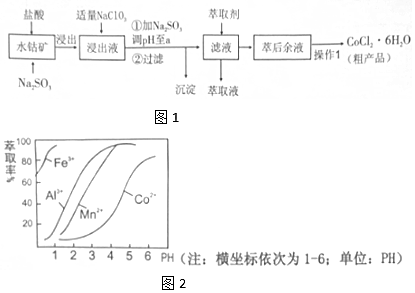
3.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、A12O3、MnO等)制取CoCl2•6H2O的工艺流程如图1:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L);
③CoCl2•6H2O熔点为86℃,加热至110〜120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)若不慎向“浸出液”中加过量NaClO2时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干需减压烘干的原因是降低烘干温度,防止产品分解.
(4)萃取剂对金属离子的萃取率与pH的关系如图2向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)为测定粗产品中CoCl2•6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L);
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)若不慎向“浸出液”中加过量NaClO2时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干需减压烘干的原因是降低烘干温度,防止产品分解.
(4)萃取剂对金属离子的萃取率与pH的关系如图2向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)为测定粗产品中CoCl2•6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答条即可)
4.下列物质转化常通过加成反应实现的是( )
| A. |  | B. | CH3CH2OH→CH3CHO | ||
| C. | CH4→CH3Cl | D. | CH2=CH2→CH3CH2Br |
20.下列反应不属于氧化还原反应的是( )
| A. | CaO+H2O=Ca(OH)2 | B. | 2Na2O2+2H2O=4NaOH+O2↑ | ||
| C. | 2Na+2H2O=2NaOH+H2↑ | D. | 4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
10.下列反应的离子方程式正确的是( )
| A. | 氧化铜跟硝酸反应:CuO+2H+═Cu2++H2O | |
| B. | NO2气体与水反应:2NO2+H2O═2H++NO3-+NO↑ | |
| C. | 硫酸和氢氧化钡溶液反应:SO42-+H++OH-+Ba2+═BaSO4↓+H2O | |
| D. | AlCl3溶液中加入氨水:Al3++3OH-═Al(OH)3↓ |
17. 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A. | 该反应的化学方程式为6A+2D?3B+4C | |
| B. | 反应进行到1s时,v(A)=v(B) | |
| C. | 反应进行到5s时,v(A)=v(B)=v(C)=v(D) | |
| D. | 反应进行到5s时,B的平均反应速率为0.06mol/(L•s) |
14.将0.1mol两种气态烃(其中一种为炔烃)组成的混合气体完全燃烧后得3.36L(标况)CO2和3.6g H2O.则这两种烃的物质的量之比说法正确的是( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 无法计算 |
15.某电池总反应为 2Fe3++Cu═2Fe2++Cu2+,不能实现该反应的原电池是( )
| A. | 电极材料 Fe、Cu,电解质溶液 FeCl3 溶液 | |
| B. | 电极材料石墨、Cu,电解质溶液 Fe2(SO4)3溶液 | |
| C. | 电极材料 Pt、Cu,电解质溶液 FeCl3溶液 | |
| D. | 电极材料 Ag、Cu,电解质溶液 Fe2(SO4)3溶液 |