题目内容
下列反应是制取某一种香料的中间过程: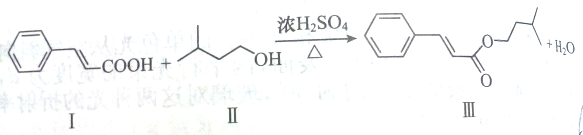
下列有关说法正确的是( )

下列有关说法正确的是( )
| A、Ⅱ物质的名称为2-甲基-4-丁醇 |
| B、Ⅲ物质的分子式为C14H18O2 |
| C、Ⅰ物质的9个碳原子一定共面 |
| D、Ⅲ物质中有3种官能团 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:A.主链编号错误;
B.根据结构检验判断元素种类和原子个数,可确定有机物的分子式;
C.根据苯、乙烯的结构特点判断;
D.Ⅲ含有碳碳双键、酯基.
B.根据结构检验判断元素种类和原子个数,可确定有机物的分子式;
C.根据苯、乙烯的结构特点判断;
D.Ⅲ含有碳碳双键、酯基.
解答:
解:A.Ⅱ物质的名称为3-甲基丁醇,故A错误;
B.由结构简式可知有机物的分子式为C14H18O2,故B正确;
C.苯环和碳碳双键之间为单键,为δ键,可旋转,所有的碳原子不一定在同一个平面上,故C错误;
D..Ⅲ含有碳碳双键、酯基两种官能团,故D错误.
故选B.
B.由结构简式可知有机物的分子式为C14H18O2,故B正确;
C.苯环和碳碳双键之间为单键,为δ键,可旋转,所有的碳原子不一定在同一个平面上,故C错误;
D..Ⅲ含有碳碳双键、酯基两种官能团,故D错误.
故选B.
点评:本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构特点以及官能团的性质,难道不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
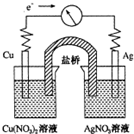 将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是( )
将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是( )| A、KNO3盐桥中的K+移向Cu(NO3)2溶液 |
| B、Ag作负极,Cu作正极 |
| C、工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大 |
| D、取出盐桥后,电流计的指针依然发生偏转 |
已知某氧化剂XO3-中+5价的X能被Na2SO3还原成0价,则还原含有2.4×10-3molXO3-的溶液,需0.2mol?L-1的Na2SO3溶液的体积为( )
| A、40mL | B、30mL |
| C、20mL | D、10mL |
H2和I2在一定条件下能发生反应:H2(g)+I2(g)═2HI(g)△H=-a kJ/mol下列说法正确的是( )
已知:
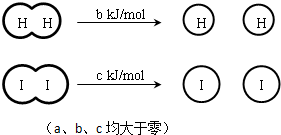
已知:

| A、H2、I2和HI分子中的化学键都是非极性共价键 |
| B、断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ |
| C、相同条件下,1 mol H2(g)和1mol I2(g)总能量小于2 mol HI (g)的总能量 |
| D、向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ |
石油是重要的能源和化工原料,我国南海因为富含石油资源而被菲律宾等邻国觊觎.下列燃料不是从石油中分离出来的是( )
| A、煤油 | B、柴油 | C、酒精 | D、汽油 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、1 mol Cl2与足量的铁反应转移的电子数是2 NA |
| B、常温常压下22.4 L HCl气体含有的分子数是NA |
| C、0.1 mol/L CuCl2溶液中Cl-数目是0.2 NA |
| D、32 g O2中含有的原子数是 NA |
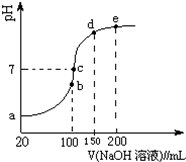 按要求回答下列问题:
按要求回答下列问题: