题目内容
14.下列各组物质中,化学键类型完全相同的是( )| A. | HI和NaI | B. | H2S和CO2 | C. | H2O2和CCl4 | D. | Na2O2和NaBr |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,如果相互作用原子是相同元素,其化学键是非极性共价键;如果是不同元素,其化学键是极性共价键.
解答 解:A.HI分子中氢原子和碘原子之间只存在极性共价键,NaI中镁离子和氯离子之间只存在离子键,所以化学键类型不同,故A错误;
B.H2S分子中硫原子和氢原子之间存在极性共价键,CO2分子中碳原子和氧原子之间存在极性共价键,所以化学键类型相同,故B正确;
C.H2O2分子中氧原子和氧原子之间存在非极性共价键,氧原子和氢原子之间存在极性共价键,CCl4分子中碳原子和氯原子之间存在极性共价键,所以化学键类型不同,故C错误;
D.Na2O2中钠离子和过氧根离子之间存在离子键、氧原子和氧原子之间存在非极性共价键,NaBr中钠离子和溴离子之间只存在离子键,所以化学键类型不同,故D错误;
故选B.
点评 本题考查了离子键和化学键的判断,根据离子键和共价键的概念来分析解答,不能根据物质所含元素判断化学键,注意氯化铵虽然全部是由非金属元素构成的,但氯化铵中含有离子键,为易错点.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
5.中学化学常用的酸碱指示剂酚酞的结构简式如图所示,列关于酚酞的说法不正确的是( )
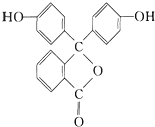

| A. | 酚酞具有弱酸性,且属于芳香族化合物 | |
| B. | 酚酞的分子式为C20H12O4 | |
| C. | 1mol酚酞最多与2molNaOH发生反应 | |
| D. | 酚酞在碱性条件下能够发生水解反应,呈现红色 |
2.下列说法正确的是( )
| A. | NO2与水的反应:3NO2+H2O═2NO3-+NO+2H+ | |
| B. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 向硅酸钠溶液中通入SO2:SiO32-+2H+═H2SiO3↓ |
9.在一定条件下,2N02?N204正反应放热,达到平衡,下列说法正确的是( )
| A. | 在密闭定容体系中降温,混合气颜色变浅,体系压强增大 | |
| B. | 只降温,混合气体颜色变浅,说明正反应是放热的 | |
| C. | 加压时,混合气颜色开始变浅,后来又逐渐加深 | |
| D. | 加压时,混合气颜色开始变深,后来又逐渐变浅 |
19.下列物质属于电解质的是( )
| A. | 铜 | B. | 氯化钠 | C. | 稀硫酸 | D. | 酒精 |
6.下列溶液中,Cl-离子浓度最大的是( )
| A. | 0.5mol•L-1HCl溶液 | B. | 1mol•L-1MgCl2溶液 | ||
| C. | 2mol•L-1NaCl溶液 | D. | 1mol•L-1FeCl3溶液 |
4.研究电化学腐蚀及防护的装置如图所示,下列有关说法正确的是( )


| A. | d为锌块,铁片腐蚀加快 | |
| B. | d为石墨,铁片不易被腐蚀 | |
| C. | d为锌块,铁片上电极反应为:2H++2e-=H2↑ | |
| D. | d为石墨,石墨上电极反应为:O2+2H2O+4e-=4OH- |
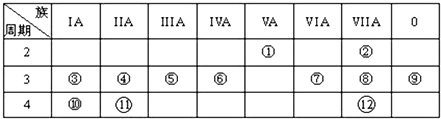
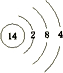 ,写出①的气态氢化物分子的电子式
,写出①的气态氢化物分子的电子式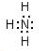 .
.