题目内容
1.下列各组物质中性质的变化规律排列正确的是( )| A. | 酸性:HClO4>H2SO4>H3PO4>H4SiO4 | B. | 稳定性:HI>HBr>HCl>HF | ||
| C. | 微粒半径:Al3+>Mg2+>Na+>F- | D. | 碱性:Ca(OH)2>KOH>Mg(OH)2>Al(OH)3 |
分析 A.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
B.元素的非金属性越强,其氢化物的稳定性越强;
C.电子层结构相同的离子,离子半径随着原子序数增大而减小;
D.元素的金属性越强,其最高价氧化物的水化物碱性越强.
解答 解:A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性Cl>S>P>Si,所以酸性:HClO4>H2SO4>H3PO4>H4SiO4,故A正确;
B.元素的非金属性越强,其氢化物的稳定性越强,非金属性I<Br<Cl<F,所以氢化物的稳定性HI<HBr<HCl<HF,故B错误;
C.电子层结构相同的离子,离子半径随着原子序数增大而减小,这几种离子电子层结构相同,且原子序数大小顺序是Al>Mg>Na>F,所以离子半径Al3+<Mg2+<Na+<F-,故C错误;
D.元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性K>Ca>Mg>Al,所以碱性:KOH>Ca(OH)2>Mg(OH)2>Al(OH)3,故D错误;
故选A.
点评 本题考查元素周期律,为高频考点,明确同一周期、同一主族元素原子结构及其性质递变规律是解本题关键,侧重考查学生分析判断能力,注意规律中的反常现象,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
19.下列判断或实验方法合理的是( )
| A. | 检验溶液中是否含有Fe2+:依次加入氯水和KSCN溶液 | |
| B. | pH=2的溶液,可能大量含有:Na+、AlO2-、CO32-、SO32- | |
| C. | 在常温下加入铝粉有氢气放出,则溶液中可能大量含有:K+、Na+、OH-、Cl- | |
| D. | 使紫色石蕊试液变红色的溶液,可能大量含有:K+、Fe2+、Cl-、NO3- |
20.下列有关电解质溶液的说法中错误的是( )
| A. | 0.1mol•L-1的HCl溶液的pH=1 | |
| B. | 0.1mol•L-1的CH3COOH溶液中c(H+)<0.1mol•L-1 | |
| C. | 0.1mol•L-1的CH3COOH溶液和0.1mol•L-1的NaOH溶液等体积混合后溶液的pH=7 | |
| D. | 100mL0.1mol•L-1的H2SO4溶液中慢慢滴入100mL0.1mol•L-1的Ba(OH)溶液后,混合溶液的导电性几乎为零 |
9.室温下,用相同浓度的NaOH溶液,分别滴定100mL浓度均为0.1mol•L-1的三种酸(HM、HN和HR)溶液,滴定的曲线如图所示,下列判断错误的是( )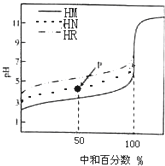

| A. | 三种酸的电离常数关系:KHM>KHN>KHR | |
| B. | pH=7时,三种溶液中:c(M-)>c(N-)>c(R-) | |
| C. | 滴定至P点时,溶液中:c(Na+)>c(N-)>c(HN)>c(H+)>c(OH-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+) |
16.下列说法中不正确的是( )
| A. | 高吸水性树脂属于功能高分子材料 | |
| B. | 聚乙烯制成的塑料可以反复加热熔融,是热塑性塑料 | |
| C. | 光导纤维、合成纤维和人造纤维都是有机高分子化合物 | |
| D. | 鉴别织物成分是真丝还是人造丝:用灼烧的方法 |
6.符合分子式C4H9Cl的同分异构体的数目为( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
13.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不.正确的是( )
| A. | 氯水的颜色呈浅黄绿色,说明氯水中含有 Cl2 | |
| B. | 向氯水中滴加硝酸酸化的 AgNO3溶液,产生白色沉淀,说明氯水中含有 Cl- | |
| C. | 向氯水中加入 NaHCO3粉末,有气泡产生,说明氯水中含有 H+ | |
| D. | 向 FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有 HClO |
10.下列指定反应的离子方程式正确的是( )
| A. | 用氯化铁溶液腐蚀铜板:Cu+Fe3+═Cu2++Fe2+ | |
| B. | 用白醋、淀粉碘化钾试纸检验加碘盐是否含碘:5I-+IO3-+6H+=3I2+3H2O | |
| C. | 向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| D. | 用洁厕剂(主要成分HCl)与大理石反应:CaCO3+2H+=Ca2++CO2↑+H2O |
11.在实验室,下列试剂通常保存在棕色试剂瓶中的是( )
| A. | 浓硫酸 | B. | 稀盐酸 | C. | 醋酸 | D. | 浓硝酸 |