题目内容
下列化学反应中,不属于氧化还原反应( )
A、2H2O2
| ||||
| B、Zn+H2SO4═ZnSO4+H2↑ | ||||
| C、CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||||
| D、Cl2+H2O═HCl+HClO |
考点:氧化还原反应
专题:氧化还原反应专题
分析:氧化还原反应的特征为有化合价的升降,反应属于氧化还原反应的变化,肯定存在化合价的变化,以此解答该题.
解答:
解:A.O元素化合价由-1价分别变为-2价、0价,为氧化还原反应,故A不选;
B.Zn和H元素化合价发生变化,属于氧化还原反应,故B不选;
C.元素化合价没有发生变化,不是氧化还原反应,故C选;
D.Cl元素化合价发生变化,属于氧化还原反应,故D不选.
故选C.
B.Zn和H元素化合价发生变化,属于氧化还原反应,故B不选;
C.元素化合价没有发生变化,不是氧化还原反应,故C选;
D.Cl元素化合价发生变化,属于氧化还原反应,故D不选.
故选C.
点评:本题考查氧化还原反应,侧重于学生的分析能力考查,为高频考点,注意把握氧化还原反应的特征,从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,难度不大.

练习册系列答案
相关题目
在某无色透明的溶液中,能共存的离子组是( )
| A、Na+、H+、SO42-、HCO3- |
| B、MnO4-、Na+、S2-、K+ |
| C、Na+、K+、Cl-、NO3- |
| D、Fe3+、K+、SO42-、Cl- |
下列装置中电流表指针会发生偏转的是( )
A、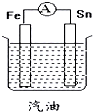 |
B、 |
C、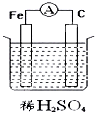 |
D、 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如图所示.Z元素原子核外K层与M层电子数相等.下列说法中正确的是( )
| X | Y | ||
| Z | W |
| A、原子半径由小到大的顺序为:Y<X<W<Z |
B、X元素最高价氧化物分子的比例模型为 |
| C、Z单质与X元素最高价氧化物、Y单质都能反应,体现氧化性 |
| D、W的单质在地壳含量丰富,是国家经济发展的重要基础原材料.2005年美国科学家发现了W的“超级原子”结构-W13 |
已知:HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是( )
| A、对比等浓度的两种酸的pH |
| B、对比等浓度的两种酸,与相同大小镁条反应的初始速率 |
| C、对比等浓度、等体积的两种酸,与等量NaOH溶液反应后放出的热量 |
| D、对比等浓度、等体积的两种酸,与足量Zn反应,生成H2的体积 |
下列有关金属腐蚀与防护的说法正确的是( )
| A、可将地下输油管与外加直流电源的正极相连以保护它不受腐蚀 |
| B、当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C、在海轮外壳连接一锌块保护外壳不受腐蚀是采用了牺牲阴极的阳极保护法 |
| D、纯银器表面在空气中因化学腐蚀渐渐变暗 |
 某研究性学习小组用如图所示装置研究不同能量之间的转化问题.下列说法正确的是( )
某研究性学习小组用如图所示装置研究不同能量之间的转化问题.下列说法正确的是( )| A、断开开关S1,按下开关S2,此时构成的装置属于电解池 |
| B、断开开关S1,按下开关S2,化学能转化为电能,电能转化为光能等 |
| C、断开开关S2,按下开关S1,此时构成的装置属于原电池 |
| D、断开开关S2,按下开关S1,化学能转化为电能 |
可逆反应N2+3H2?2NH3(各物质均为气体)的正、逆反应速率可用单位时间内各反应物或生成物浓度的变化来表示.下列各关系中能说明该反应已达到平衡状态的是( )
| A、3v正(N2)=v正(H2) |
| B、v正(N2)=v逆(NH3) |
| C、2 v正(H2)=3 v逆(NH3) |
| D、2v逆(NH3)=3 v正(H2) |