题目内容
19.写出甲醇燃料电池在碱性氢氧化钾中反应的方程式:2CH3OH+3O2+4KOH=2K2CO3+6H2O.分析 甲醇燃料电池中,负极上甲醇失去电子发生氧化反应,正极上氧气得电子发生还原反应,总反应式为甲醇燃烧的方程式.
解答 解:甲醇燃料碱性电池中,甲醇在负极上发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,通入氧气的极为原电池的正极,正极上发生还原反应O2+4e-+2H2O=4OH-;总反应式两极反应加和,即2CH3OH+3O2+4KOH=2K2CO3+6H2O.
故答案为:2CH3OH+3O2+4KOH=2K2CO3+6H2O.
点评 本题考查了电极反应式的书写知识,难度不大,注意燃料电池中电极反应式的书写要结合电解质溶液的酸碱性,虽然燃料和氧化剂相同,如果电解质溶液不同,则电极反应式就不同.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
10.有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液的实验如下:
由此判断,下列说法正确的是( )
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴甲基橙 | 溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓硫酸,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| (4)取(3)中的上层清液,加AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| (5)取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
| A. | 根据实验(1)可以确定溶液中不含有HCO3-和I-,因为这二个离子相对应的酸为弱酸 | |
| B. | 溶液中一定存在的离子是NO3-、SO42-、Cl-、Mg2+、Al3+;溶液中肯定不存在的离子是:Fe2+、HCO3-、I-、Ba2+ | |
| C. | 为进一步确定其它离子,应该补充焰色反应的实验来检验K+就可以 | |
| D. | 通过实验(1)和(2)就可以确定溶液中一定含有NO3-,一定不含有Fe2+、I-、HCO3-,所以实验步骤(4)的设计是错误的 |
11. 以Pt为电极电解淀粉KI溶液的装置如图所示,中间用阴离子交换膜(只允许阴离子通过)将电解槽隔开,则下列观点正确的是( )
以Pt为电极电解淀粉KI溶液的装置如图所示,中间用阴离子交换膜(只允许阴离子通过)将电解槽隔开,则下列观点正确的是( )
 以Pt为电极电解淀粉KI溶液的装置如图所示,中间用阴离子交换膜(只允许阴离子通过)将电解槽隔开,则下列观点正确的是( )
以Pt为电极电解淀粉KI溶液的装置如图所示,中间用阴离子交换膜(只允许阴离子通过)将电解槽隔开,则下列观点正确的是( )| A. | 电解过程中左侧发生的电极反应式:40H--4e-═2H2O+O2↑ | |
| B. | 电解过程中左侧溶液中的0H-通过离子交换膜向右侧溶液移动 | |
| C. | 电解一段时间后左、右两侧溶液中的K+的物质的量浓度不变 | |
| D. | 电解初期,右侧溶液能变蓝色,继续电解,溶液的蓝色一定加深 |
10.下列物质中只含有共价键的化合物是( )
| A. | NaOH | B. | MgCl2 | C. | N2 | D. | H2O2 |




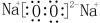 .
. .
.