题目内容
核外电子数为1~18的元素中,下列叙述正确的是( )
| A、最外层只有1个电子的元素,一定是金属元素 |
| B、最外层只有2个电子的元素,一定是金属元素 |
| C、原子核外电子层数与最外层电子数相等的元素,一定是金属元素 |
| D、核电荷数为17的元素的原子容易获得1个电子 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:A、氢元素最外层只有一个电子;
B、氦元素最外层2个电子;
C、氢元素最外层只有一个电子,电子层数与最外层电子数相等;
D、核电荷数为17的元素最外层有7个电子.
B、氦元素最外层2个电子;
C、氢元素最外层只有一个电子,电子层数与最外层电子数相等;
D、核电荷数为17的元素最外层有7个电子.
解答:
解:A、氢元素最外层只有一个电子,是非金属元素,故A错误;
B、氦元素最外层2个电子,是稀有气体元素,故B错误;
C、氢元素最外层只有一个电子,电子层数与最外层电子数相等,是非金属元素,故C错误;
D、核电荷数为17的元素最外层有7个电子,易得1个电子达8电子的稳定结构,故D正确;
故选D.
B、氦元素最外层2个电子,是稀有气体元素,故B错误;
C、氢元素最外层只有一个电子,电子层数与最外层电子数相等,是非金属元素,故C错误;
D、核电荷数为17的元素最外层有7个电子,易得1个电子达8电子的稳定结构,故D正确;
故选D.
点评:本题考查元素周期表的结构及应用,为高频考点,把握周期表结构及元素的位置、元素的种类为解答的关键,侧重基础知识的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
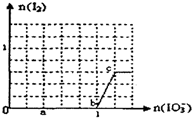 已知:还原性HSO3?>I?,氧化性IO3?>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )
已知:还原性HSO3?>I?,氧化性IO3?>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )| A、反应过程中的氧化产物均为SO42- |
| B、a点时剩余NaHSO3的物质的量为1.8 mol |
| C、c点时的还原产物可能是KI或NaI |
| D、当溶液中I?与I2的物质的量之比为1:1时,加入的KIO3为1.2mol |
元素X、Y可组成化学式为XY2的离子化合物,则X、Y的原子序数可能是( )
| A、12和9 | B、6和16 |
| C、13和17 | D、11和17 |
同主族元素形成的同一类型化合物,往往其结构和性质相似.PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是( )
| A、它是一种共价化合物 |
| B、它既含离子键又含共价键 |
| C、它不可能与NaOH溶液反应 |
| D、它受热时难以分解 |
向含有 1molKAl(SO4)2的溶液中加入Ba(OH)2溶液,使SO42-恰好完全沉淀,此时Al(OH)3的物质的量为( )
| A、1mol | B、1.33mol |
| C、1.67mol | D、0 |
下列叙述正确的是( )
| A、共价化合物一定都是由非金属构成 |
| B、含有共价键的化合物都是共价化合物 |
| C、HCl=H++Cl-,故HCl是离子化合物 |
| D、凡是含有离子键的化合物都是离子化合物 |
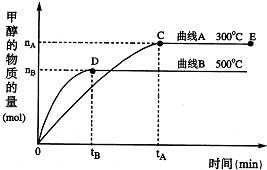 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)═CH3OH(g)
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)═CH3OH(g)