题目内容
下列各组离子在指定溶液中,能大量共存的是
①无色溶液中:K+ Cl-,Ca2+,CO32-,SO42-,NO3-
②pH=11的溶液中:CO32-,Na+,AlO2-,NO3-,S2-,SO32-
③水电离的H+浓度c(H+)=10-12mol?L-1的溶液中:Cl-,CO32-,NO3-,NH4+,SO32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-,S2O32-
⑤使石蕊变红的溶液中:Fe2+,MnO4-,NO3-,Na+,SO42-
⑥中性溶液中:Fe3+,Al3+,NO3-,I-,Cl-,S2-( )
①无色溶液中:K+ Cl-,Ca2+,CO32-,SO42-,NO3-
②pH=11的溶液中:CO32-,Na+,AlO2-,NO3-,S2-,SO32-
③水电离的H+浓度c(H+)=10-12mol?L-1的溶液中:Cl-,CO32-,NO3-,NH4+,SO32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-,S2O32-
⑤使石蕊变红的溶液中:Fe2+,MnO4-,NO3-,Na+,SO42-
⑥中性溶液中:Fe3+,Al3+,NO3-,I-,Cl-,S2-( )
| A、② | B、①③⑥ | C、②④ | D、①②⑤ |
考点:离子共存问题
专题:
分析:①钙离子与碳酸根离子、硫酸根离子反应生成沉淀;
②pH=11的溶液为碱性溶液,CO32-,Na+,AlO2-,NO3-,S2-,SO32-离子之间不发生反应,也不与氢氧根离子反应;
③水电离的氢离子浓度c(H+)=10-12mol?L-1的溶液为酸性或者碱性溶液,铵根离子与氢氧根离子反应,碳酸根离子、亚硫酸根与氢离子反应,硝酸根离子在酸性条件下能够氧化亚硫酸根离子;
④加入Mg能放出氢气的溶液中存在大量氢离子,硫代硫酸根离子与氢离子反应;
⑤使石蕊变红的溶液为酸性溶液,高锰酸根离子、硝酸根离子在酸性条件下能够氧化亚铁离子;
⑥中性溶液中,铁离子、铝离子水解溶液溶液不会显示中性;且铁离子能够氧化碘离子、硫离子,铝离子与硫离子发生双水解反应.
②pH=11的溶液为碱性溶液,CO32-,Na+,AlO2-,NO3-,S2-,SO32-离子之间不发生反应,也不与氢氧根离子反应;
③水电离的氢离子浓度c(H+)=10-12mol?L-1的溶液为酸性或者碱性溶液,铵根离子与氢氧根离子反应,碳酸根离子、亚硫酸根与氢离子反应,硝酸根离子在酸性条件下能够氧化亚硫酸根离子;
④加入Mg能放出氢气的溶液中存在大量氢离子,硫代硫酸根离子与氢离子反应;
⑤使石蕊变红的溶液为酸性溶液,高锰酸根离子、硝酸根离子在酸性条件下能够氧化亚铁离子;
⑥中性溶液中,铁离子、铝离子水解溶液溶液不会显示中性;且铁离子能够氧化碘离子、硫离子,铝离子与硫离子发生双水解反应.
解答:
解:①无色溶液中不存在有色离子,Ca2+与SO42-、CO32-之间反应生成沉淀,在溶液中不能大量共存,故①错误;
②pH=11的溶液中存在大量氢氧根离子,CO32-,Na+,AlO2-,NO3-,S2-,SO32-离子之间不反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故②正确;
③水电离的氢离子浓度c(H+)=10-12mol?L-1的溶液中存在大量氢离子或氢氧根离子酸性溶液中CO32-,SO32-与氢离子反应,碱性溶液中,NH4+与氢氧根离子反应,在溶液中不能大量共存,故③错误;
④加入Mg能放出H2的溶液为酸性溶液,S2O32-根离子与氢离子反应生成硫单质和二氧化硫气体,在溶液中不能大量共存,故④错误;
⑤使石蕊变红的溶液中存在大量氢离子,MnO4-、NO3-在酸性溶液中具有强氧化性,能够氧化Fe2+,在溶液中不能大量共存,故⑤错误;
⑥Fe3+、Al3+与S2-发生双水解反应,Fe3+能够氧化I-、S2-,在溶液中不能大量共存,故⑥错误;
根据以上分析可知,正确的只有②,
故选A.
②pH=11的溶液中存在大量氢氧根离子,CO32-,Na+,AlO2-,NO3-,S2-,SO32-离子之间不反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故②正确;
③水电离的氢离子浓度c(H+)=10-12mol?L-1的溶液中存在大量氢离子或氢氧根离子酸性溶液中CO32-,SO32-与氢离子反应,碱性溶液中,NH4+与氢氧根离子反应,在溶液中不能大量共存,故③错误;
④加入Mg能放出H2的溶液为酸性溶液,S2O32-根离子与氢离子反应生成硫单质和二氧化硫气体,在溶液中不能大量共存,故④错误;
⑤使石蕊变红的溶液中存在大量氢离子,MnO4-、NO3-在酸性溶液中具有强氧化性,能够氧化Fe2+,在溶液中不能大量共存,故⑤错误;
⑥Fe3+、Al3+与S2-发生双水解反应,Fe3+能够氧化I-、S2-,在溶液中不能大量共存,故⑥错误;
根据以上分析可知,正确的只有②,
故选A.
点评:本题考查离子共存的判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;注意明确题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
对于在一密闭容器中进行的下列反应:C(s)+O2(g)?CO2(g)下列说法中错误的是( )
| A、将木炭粉碎成粉末状可以加快化学反应速率 |
| B、升高温度可以加快化学反应速率 |
| C、增加压强不能加快化学反应速率 |
| D、增加木炭的量可以加快化学反应速率 |
下列实验操作或检验正确的是( )
A、 收集氯气 |
B、 模拟石油蒸馏 |
C、 转移溶液 |
D、 用海水制少量蒸馏水 |
实验室需要配制2mol/l的NaCl溶液450ml,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
| A、450ml,52.65g |
| B、任意规格,52.65g |
| C、500 ml,58.5g |
| D、1000 ml,117g |

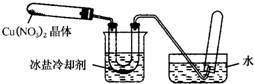 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质.
某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质.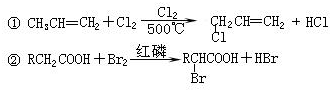
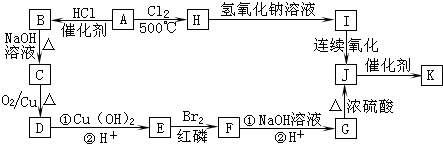
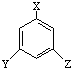 ,又能发生银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有
,又能发生银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有