题目内容
(1)下列表示物质结构的化学用语或模型图正确的是:(双选)
A.10B20的原子核外电子排布为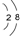
B.氯化钠的电子式为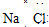
C.重水的化学式为
H2O(或D2O)
D.
Li和
Li互为同位素
E.氯化钙电子式: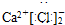
F.硫化钠电子式: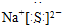
G.互为同分异构体:O2和O3
(2)用电子式表示下列物质的结构:
①Na2O2 ,②HCl .
(3)有以下10种物质:属于电解质的是 ;属于非电解质的是 .
①铜 ②稀硫酸 ③氯化氢 ④氨气 ⑤空气⑥二氧化碳 ⑦金属汞(俗称水银) ⑧氯化钠 ⑨硫酸钡 ⑩氯气.
A.10B20的原子核外电子排布为
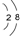
B.氯化钠的电子式为
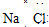
C.重水的化学式为
2 1 |
D.
6 3 |
7 3 |
E.氯化钙电子式:
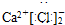
F.硫化钠电子式:
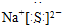
G.互为同分异构体:O2和O3
(2)用电子式表示下列物质的结构:
①Na2O2
(3)有以下10种物质:属于电解质的是
①铜 ②稀硫酸 ③氯化氢 ④氨气 ⑤空气⑥二氧化碳 ⑦金属汞(俗称水银) ⑧氯化钠 ⑨硫酸钡 ⑩氯气.
考点:电子式、化学式或化学符号及名称的综合,电解质与非电解质
专题:化学用语专题,电离平衡与溶液的pH专题
分析:(1)A.10B20表示20个B原子的质量数为10,该元素为H元素,核外电子总数为1;
B.氯化钠为离子化合物,电子式中需要标出阴阳离子所带电荷;
C.重水分子中含有2个D原子和一个O原子,其中D原子可以表示为
H;
D.
Li和
Li的核电荷数相同、中子数不同,二者互为同位素;
E.氯化钙的电子式中,两个氯离子不能合并,氯离子应该分别写在钙离子的两边;
F.硫化钠的电子式中含有两个钠离子;
G.互为同分异构体的物质必须具有相同的分子式、不同结构,氧气和臭氧的分子式不同,二者为同素异形体.
(2)①过氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,注意过氧根离子的表示方法;
②氯化氢为共价化合物,分子中存在1个氢氯共用电子对,氯原子最外层达到8电子稳定结构,氢原子最外层为2个电子;
(3)在水溶液或熔融状态下能够导电的化合物为电解质,在水溶液和熔融状态下都不能导电的化合物为非电解质,单质和混合物既不是电解质,也不是非电解质.
B.氯化钠为离子化合物,电子式中需要标出阴阳离子所带电荷;
C.重水分子中含有2个D原子和一个O原子,其中D原子可以表示为
2 1 |
D.
6 3 |
7 3 |
E.氯化钙的电子式中,两个氯离子不能合并,氯离子应该分别写在钙离子的两边;
F.硫化钠的电子式中含有两个钠离子;
G.互为同分异构体的物质必须具有相同的分子式、不同结构,氧气和臭氧的分子式不同,二者为同素异形体.
(2)①过氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,注意过氧根离子的表示方法;
②氯化氢为共价化合物,分子中存在1个氢氯共用电子对,氯原子最外层达到8电子稳定结构,氢原子最外层为2个电子;
(3)在水溶液或熔融状态下能够导电的化合物为电解质,在水溶液和熔融状态下都不能导电的化合物为非电解质,单质和混合物既不是电解质,也不是非电解质.
解答:
解:(1)A.10B20表示20个B原子的质量数为10,该元素为H元素,氢原子的结构示意图为: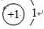 ,故A错误;
,故A错误;
B.氯化钠属于离子化合物,钠离子直接用离子符号表示,阴离子需要标出所带电荷及最外层电子,氯化钠正确的电子式为: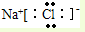 ,故B错误;
,故B错误;
C.重水分子中含有2个D原子和一个O原子,其中D原子可以表示为
H,重水的分子式为:
H2O(或D2O),故C正确;
D.
Li和
Li具有相同的核电荷数、不同的中子数,二者互为同位素,故D正确;
E.氯化钙为离子化合物,其电子式中,两个氯离子不能合并,氯化钙正确的电子式为: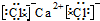 ,故E错误;
,故E错误;
F.硫化钠的化学式中含有两个钠离子,硫化钠正确的电子式为: ,故F正确;
,故F正确;
G.O2和O3的分子式不同,二者为同素异形体,不属于同分异构体,故G错误;
故答案为:CD;
(2)①Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为: ,
,
故答案为: ;
;
②氯化氢属于共价化合物,分子中存在1个氢氯键,氯化氢的电子式为: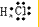 ,
,
故答案为: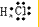 ;
;
(3)电解质为:在水溶液或熔融状态下能够导电的化合物,满足条件的有:③氯化氢、⑧氯化钠、⑨硫酸钡;
非电解质为:在水溶液和熔融状态下都不能导电的化合物,满足条件的有:④氨气、⑥二氧化碳,
故答案为:③⑧⑨; ④⑥.
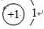 ,故A错误;
,故A错误;B.氯化钠属于离子化合物,钠离子直接用离子符号表示,阴离子需要标出所带电荷及最外层电子,氯化钠正确的电子式为:
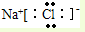 ,故B错误;
,故B错误;C.重水分子中含有2个D原子和一个O原子,其中D原子可以表示为
2 1 |
2 1 |
D.
6 3 |
7 3 |
E.氯化钙为离子化合物,其电子式中,两个氯离子不能合并,氯化钙正确的电子式为:
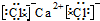 ,故E错误;
,故E错误;F.硫化钠的化学式中含有两个钠离子,硫化钠正确的电子式为:
 ,故F正确;
,故F正确;G.O2和O3的分子式不同,二者为同素异形体,不属于同分异构体,故G错误;
故答案为:CD;
(2)①Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为:
 ,
,故答案为:
 ;
;②氯化氢属于共价化合物,分子中存在1个氢氯键,氯化氢的电子式为:
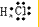 ,
,故答案为:
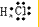 ;
;(3)电解质为:在水溶液或熔融状态下能够导电的化合物,满足条件的有:③氯化氢、⑧氯化钠、⑨硫酸钡;
非电解质为:在水溶液和熔融状态下都不能导电的化合物,满足条件的有:④氨气、⑥二氧化碳,
故答案为:③⑧⑨; ④⑥.
点评:本题考查了常见化学用语的书写判断、电解质与非电解质的判断,题目难度中等,试题内容较多,中心较强,注意掌握常见化学用语的概念及正确的表示方法,明确电解质与非电解质的区别,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-,现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.792L(已换算成标准状况,且设气体全部逸出);②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.根据上述实验,以下推测正确的是( )
| A、一定不存在Ba2+,NH4+可能存在 |
| B、一定不存在Cl- |
| C、一定存在Na+ |
| D、可能存在Cl-、Na+ |
某废水含有下列离子中的5种(忽略水的电离及离子的水解),K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,测得各种离子的物质的量浓度相等.为探究废水的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
| A、溶液中无法确定Al3+的存在与否 |
| B、原溶液中不含的离子为:K+、Al3+、CO32- |
| C、步骤②中可以确定Fe2+、NO3-的存在 |
| D、步骤③中共有2种钡盐沉淀 |
肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气.
已知:N2(g)+2O2(g)=N2O4(g);△H=+8.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
已知:N2(g)+2O2(g)=N2O4(g);△H=+8.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
| A、2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1076.7 kJ/mol | ||||
B、N2H4(g)+
| ||||
| C、2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-542.7 kJ/mol | ||||
| D、2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1059.3 kJ/mol |
石灰石是一种化工原料,可以通过反应生成一系列物质,如图.
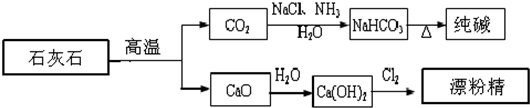
下列说法正确的是( )

下列说法正确的是( )
| A、漂粉精是混合物,主要成分是氯化钙 |
| B、图示的制纯碱方法,要求先向饱和食盐水中通NH3,然后再通CO2 |
| C、纯碱属于碱,俗名苏打 |
| D、制取纯碱和漂粉精所涉及的反应都是非氧化还原反应 |
下列溶液中氯离子浓度最大的是( )
| A、1L1mol/LAlCl3溶液中 |
| B、2L1mol/LFeCl3溶液中 |
| C、1L2mol/LKCl溶液中 |
| D、2L3mol/LMgCl2溶液中 |
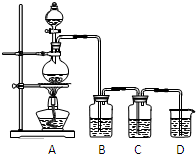 已知单质硫是淡黄色粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知单质硫是淡黄色粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: