题目内容
11.胶体遇到强电解质会发生聚沉,将某溶液逐滴加入Fe(OH)3胶体(胶粒带正电荷)中,开始时产生沉淀,继续滴加则沉淀溶解,那么该溶液是( )| A. | 2 mol•L-1 NaOH溶液 | B. | 2 mol•L-1HCl溶液 | ||
| C. | 2 mol•L-1NaCl溶液 | D. | 硅酸胶体(胶粒带负电荷) |
分析 Fe(OH)3胶体中加入电解质溶液发生聚沉生成Fe(OH)3沉淀,根据Fe(OH)3的性质来分析能继续溶解Fe(OH)3的物质.
解答 解:A.胶体中加电解质溶液发生聚沉生成Fe(OH)3沉淀,Fe(OH)3不能溶解在氢氧化钠溶液中,故A错误;
B.胶体中加电解质溶液发生聚沉生成Fe(OH)3沉淀,Fe(OH)3会溶解在盐酸溶液中,故B正确;
C.胶体中加电解质溶液发生聚沉生成Fe(OH)3沉淀,Fe(OH)3不会溶解在氯化钠溶液中,故C错误;
D.硅酸胶体中的胶粒带负电,故能和氢氧化铁胶体发生聚沉,但由于硅酸的酸性极弱,故不能使氢氧化铁沉淀溶解,故D错误.
故选B.
点评 本题考查了胶体的性质及Fe(OH)3的性质,难度不大,明确氢氧化铁不溶于水,但能溶解在强酸溶液中是解答本题的关键.

练习册系列答案
相关题目
4.等质量的CuO和MgO粉末分别溶于相同体积的足量硝酸中,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为amol•L-1和bmol•L-1.则a与b的关系为( )
| A. | a=b | B. | a=2b | C. | 2a=b | D. | 无法确定 |
4.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 糖和水 | B. | 盐和水 | C. | 菜油和水 | D. | 苏打和水 |
1.对于反应2A2+B2=2A2B,已知A2、B2、A2B的键能如下表
当2molA2完全反应吸收(填“放出”或“吸收”)热量226KJ.
| 化学键 | A-A | B=B | A-B |
| 键能kJ/mol | 236 | 406 | 163 |
16.下列溶液中的氯离子浓度与50mL 1mol/L的AlCl3溶液中氯离子浓度相等的是( )
| A. | 75 mL 2 mol/L的CaCl2 | B. | 100 mL 2 mol/L的NH4Cl | ||
| C. | 150 mL 1mol/L的KCl | D. | 100 mL 3 mol/L的NaCl |
3.下表列出了除去物质中所含有少量杂质的方法,其中错误的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO | CO2 | 通入足量的氢氧化钠溶液,干燥 |
| B | NaCl | 泥沙 | 加入足量的水溶解、过滤、蒸发 |
| C | NaOH溶液 | Na2CO3 | 加入足量的稀盐酸至不再产生气泡 |
| D | FeCl2溶液 | CuCl2 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
20.关于下列四个装置图的说法,正确的是( )
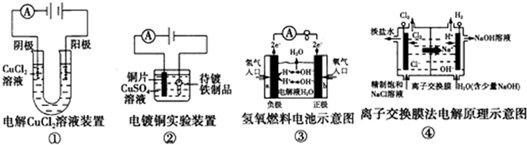

| A. | ①装置中阴极处产生的气体能够使湿润的淀粉KI试纸变蓝 | |
| B. | ②装置不能完成在铁制品上镀铜 | |
| C. | ③装置中电子由b极流向a极 | |
| D. | ④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |

 离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为( )
离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为( )