题目内容
2.下列物质熔化时不需要破坏化学键的是( )| A. | NaOH | B. | SiO2 | C. | Mg | D. | CH4 |
分析 发生化学反应时物质中的化学键被破坏,熔化及电离过程中化学键也被破坏,以此来分析.
解答 解:A.氢氧化钠属于离子晶体,熔化时破坏离子键,故A错误;
B.二氧化硅是原子晶体,熔化需要破坏共价键,故B错误;
C.金属镁属于金属晶体,熔化时破坏金属键,故C错误;
D.甲烷属于分子晶体,熔化时破坏分子间作用力,没有破坏化学键,故D正确;
故选D.
点评 本题考查化学键,熟悉化学反应中、熔化、电离过程中的化学键变化是解答本题的关键,并注意利用分子间作用力不属于化学键来解答,题目难度不大.

练习册系列答案
相关题目
13.与 3-甲基-1-戊烯同属烯烃且主链为4个碳的同分异构体共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
10.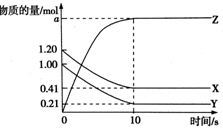 已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
 已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )| A. | a为1.60 | |
| B. | X和Y的转化率相等 | |
| C. | 0~10min的平均速率V(Z)=0.079mol•L-1•min-1 | |
| D. | 容器内Z的浓度最大可以达到1.00 mol/L |
17.历史最久的海水淡化方法是( )
| A. | 蒸馏法 | B. | 电渗析法 | C. | 离子交换法 | D. | 过滤法 |
7.下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
(1)写出⑧的原子结构示意图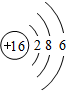 .
.
(2)④、⑤、⑥的原子半径由大到小的顺序为Na>Al>O(用元素符号回答).
(3)②、③、⑦的最高价含氧酸的酸性由强到弱顺序是HNO3>H2CO3>H2SiO3(用化学式回答)
(4)③元素所形成单质的结构式为N≡N.
(5)⑥的单质与①、⑨两种元素形成化合物的水溶液反应的离子方程式为:2Al+6H+=2Al3++3H2↑.
(6)⑤元素与⑨元素形成的化合物中,化学键类型为离子键.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
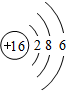 .
.(2)④、⑤、⑥的原子半径由大到小的顺序为Na>Al>O(用元素符号回答).
(3)②、③、⑦的最高价含氧酸的酸性由强到弱顺序是HNO3>H2CO3>H2SiO3(用化学式回答)
(4)③元素所形成单质的结构式为N≡N.
(5)⑥的单质与①、⑨两种元素形成化合物的水溶液反应的离子方程式为:2Al+6H+=2Al3++3H2↑.
(6)⑤元素与⑨元素形成的化合物中,化学键类型为离子键.
14.含有共价键的分子晶体是( )
| A. | NaOH | B. | SiO2 | C. | Cl2 | D. | NH4Cl |
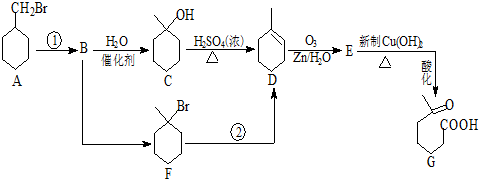
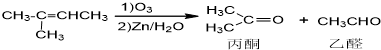
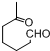 +NaOH+2Cu(OH)2$\stackrel{△}{→}$
+NaOH+2Cu(OH)2$\stackrel{△}{→}$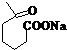 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.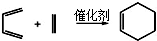
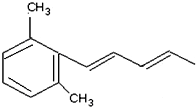
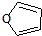 )也可以发生“Diels-Alder反应”,该化学方程式为:
)也可以发生“Diels-Alder反应”,该化学方程式为: